题目内容
7.在36g碳不完全燃烧所得气体中,CO占$\frac{1}{3}$体积,CO2占$\frac{2}{3}$体积.且有:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5kJ•mol-1
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283kJ•mol-1
与这些碳完全燃烧相比,损失的热量是( )
| A. | 172.5 kJ | B. | 1 149 kJ | C. | 283 kJ | D. | 517.5 kJ |
分析 碳不完全燃烧损失的热量为生成的一氧化碳燃烧放出的热量.根据碳原子守恒计算出一氧化碳的物质的量,再根据一氧化碳燃烧的热化学方程式计算.
解答 解:36g碳的物质的量为$\frac{36g}{12g/mol}$=3mol,
所以CO的物质的量为3mol×$\frac{1}{3}$=1mol,
由于CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283kJ/mol,所以1molCO燃烧放出的热量为283kJ/mol×1mol=283kJ.
即36g碳不完全燃烧生成1molCO损失的热量为283kJ.
故选C.
点评 本题考查反应热的计算,难度中等,关键在于清楚碳不完全燃烧损失的热量为生成的一氧化碳燃烧放出的热量.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L | |
| B. | 从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液中氢离子的浓度为2 mol/L | |
| C. | 配制480 mL 0.5 mol/L的CuSO4溶液,需称取62.5 g胆矾 | |
| D. | 中和100 mL 1mol/L的H2SO4溶液,需NaOH为4 g |
15.下列实验操作中,正确的是( )
| A. | 为了使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动 | |
| B. | 分液时,分液漏斗中的两层液体均从下口放出 | |
| C. | 为加速固体物质的溶解可采用研磨、振荡、搅拌、加热等方法 | |
| D. | 为增大气体物质的溶解度,常采用搅拌,加热等措施 |
2.社会实践活动中,课外兴趣小组对某钢铁厂的铁矿石样品和钢样进行实验、分析、计算,了解了该钢铁厂生产原料、产品的相关信息.下面请你根据他们的实验帮助计算回答:
取该厂的某钢样粉末28.36g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3g白色沉淀.
(1)计算此钢样粉末中铁和碳的质量之比.
(2)再取三份不同质量的钢样粉末分别加到50 g质量分数相同的硫酸中,充分反应后,测得的实验数据如下表所示:(标准状况下,2g H2的体积为22.4 L)
请根据表中数据计算硫酸中H2SO4的质量分数.
(3)若在实验Ⅱ中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
取该厂的某钢样粉末28.36g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3g白色沉淀.
(1)计算此钢样粉末中铁和碳的质量之比.
(2)再取三份不同质量的钢样粉末分别加到50 g质量分数相同的硫酸中,充分反应后,测得的实验数据如下表所示:(标准状况下,2g H2的体积为22.4 L)
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.836 | 5.672 | 8.508 |
| 生成气体的体积(标准状况)/L | 1.12 | 2.24 | 2.80 |
(3)若在实验Ⅱ中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
12.下列离子方程式书写正确的是( )
| A. | 用醋酸除水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 向次氯酸钙溶液中通入少量SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO | |
| C. | 碘化亚铁溶液中通入少量氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | 硝酸亚铁溶液中滴加稀硫酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
19.2010年10月16日,一场大雾袭击了京珠高速,导致京珠高速东西湖段接连发生数十起连环车祸.其中雾属于下列分散系中的( )
| A. | 溶液 | B. | 悬浊液 | C. | 乳浊液 | D. | 胶体 |
16.在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A. | Mg2+、Na+、SO42-、Cl- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | Na+、K+、OH-、Cl- | D. | Ba2+、CO32-、NO3-、K+ |

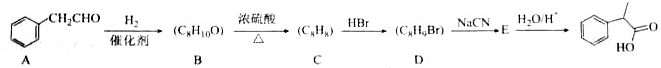
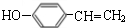 .
.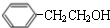 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$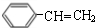 +H2O;C→D的反应类型为加成反应
+H2O;C→D的反应类型为加成反应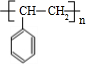 .
.