题目内容
已知:
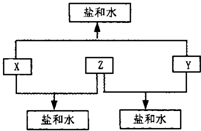
①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z.元素Y、X、Z的原子序数依次递增.
②X在A、B、C、D中都不呈现它的最高化合价.
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C.
④化合物D受热催化分解,可制得元素Y的单质.
(1)元素X是
(2)写出③中反应的化学方程式:
(3)写出④中反应的化学方程式: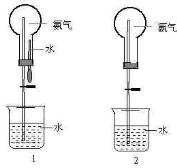
Ⅱ.制取氨气并完成喷泉实验(图中夹持装置均已略去).
(1)写出实验室制取氨气前化学方程式:
(2)收集氨气应使用
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是
(4)如果只提供如图2的装置,请说明引发喷泉的方法.
①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z.元素Y、X、Z的原子序数依次递增.
②X在A、B、C、D中都不呈现它的最高化合价.
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C.
④化合物D受热催化分解,可制得元素Y的单质.
(1)元素X是
Cl(或氯)
Cl(或氯)
,Z是K(或钾)
K(或钾)
.(2)写出③中反应的化学方程式:
Cl2+2KOH=KCl+KClO+H2O
Cl2+2KOH=KCl+KClO+H2O
.(3)写出④中反应的化学方程式:
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
.
| ||
| △ |

Ⅱ.制取氨气并完成喷泉实验(图中夹持装置均已略去).
(1)写出实验室制取氨气前化学方程式:
2NH4Cl+Ca(OH)2═2NH3↑+CaCl2+2H2O
2NH4Cl+Ca(OH)2═2NH3↑+CaCl2+2H2O
.(2)收集氨气应使用
向下排空气
向下排空气
法,要得到干燥的氨气可选用碱石灰
碱石灰
做干燥剂.(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是
打开止水夹,挤出胶头滴管中的水.
打开止水夹,挤出胶头滴管中的水.
.该实验的原理是氨气极易溶解于水,致使烧瓶内气体压强迅速减小.
氨气极易溶解于水,致使烧瓶内气体压强迅速减小.
.(4)如果只提供如图2的装置,请说明引发喷泉的方法.
打开夹子,用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,即发生喷泉
打开夹子,用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,即发生喷泉
.分析:Ⅰ.此题的突破口是:室温下单质A与某种常见一元强碱溶液反应,可得到B和C,且A、B、C中都含有X,说明A中碱中发生了歧化反应,常温下能与碱溶液发生歧化反应的在中学化学中主要是Cl2、Br2等,这就缩小了思考的范围.再结合其他条件从而找出答案.
Ⅱ.实验室制氨气由氯化铵和熟石灰在加热条件下反应,根据氨气的性质,密度比空气小,极易溶于水,为碱性气体等可找出答案;从形式喷泉实验的原理考虑,要形成喷泉,必须使圆底烧瓶内的压强比外界大气压小才可以,据此回答.
Ⅱ.实验室制氨气由氯化铵和熟石灰在加热条件下反应,根据氨气的性质,密度比空气小,极易溶于水,为碱性气体等可找出答案;从形式喷泉实验的原理考虑,要形成喷泉,必须使圆底烧瓶内的压强比外界大气压小才可以,据此回答.
解答:解:Ⅰ.(1)室温下单质A与某种常见一元强碱溶液反应,可得到B和C,且A、B、C中都含有X,说明A中碱中发生了歧化反应,常温下能与碱溶液发生歧化反应的在中学化学中主要是
Cl2、Br2等,化合物D受热催化分解,可制得元素Y的单质,可知应为KClO3,由此可知X为O,Y为Cl,Z为K,A为Cl2,D为KClO3,故答案为:Cl(或氯);K(或钾);
(2)Cl2在碱性溶液中发生自身氧化还原反应,生成KCl和KClO,故答案为:Cl2+2KOH═KCl+KClO+H2O;
(3)KClO3在催化剂条件加热分解生成O2,根据质量守恒定律可写出化学方程式,故答案为:2KClO3
2KCl+3O2↑;
Ⅱ.(1)实验室制氨气由氯化铵和熟石灰在加热条件下反应生成氨气和水,根据质量守恒定律可写出化学方程式,故答案为:2NH4Cl+Ca(OH)2═2NH3↑+CaCl2+2H2O;
(2)氨气密度比空气小,极易溶于水,只能用向下排空法收集,氨气为碱性气体,应用碱性干燥剂干燥,故答案为:向下排空气; 碱石灰;
(3)根据氨气极易溶于水,打开止水夹,挤出胶头滴管中的水时,烧瓶内压强迅速减小,外界大气压可将烧杯中的水压进烧瓶中形成喷泉,故答案为:打开止水夹,挤出胶头滴管中的水. 氨气极易溶解于水,致使烧瓶内气体压强迅速减小;
(4)如果用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,烧瓶内压强迅速减小,外界大气压可将烧杯中的水压进烧瓶中形成喷泉,故答案为:打开夹子,用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,即发生喷泉.
Cl2、Br2等,化合物D受热催化分解,可制得元素Y的单质,可知应为KClO3,由此可知X为O,Y为Cl,Z为K,A为Cl2,D为KClO3,故答案为:Cl(或氯);K(或钾);
(2)Cl2在碱性溶液中发生自身氧化还原反应,生成KCl和KClO,故答案为:Cl2+2KOH═KCl+KClO+H2O;
(3)KClO3在催化剂条件加热分解生成O2,根据质量守恒定律可写出化学方程式,故答案为:2KClO3
| ||
| △ |
Ⅱ.(1)实验室制氨气由氯化铵和熟石灰在加热条件下反应生成氨气和水,根据质量守恒定律可写出化学方程式,故答案为:2NH4Cl+Ca(OH)2═2NH3↑+CaCl2+2H2O;
(2)氨气密度比空气小,极易溶于水,只能用向下排空法收集,氨气为碱性气体,应用碱性干燥剂干燥,故答案为:向下排空气; 碱石灰;
(3)根据氨气极易溶于水,打开止水夹,挤出胶头滴管中的水时,烧瓶内压强迅速减小,外界大气压可将烧杯中的水压进烧瓶中形成喷泉,故答案为:打开止水夹,挤出胶头滴管中的水. 氨气极易溶解于水,致使烧瓶内气体压强迅速减小;
(4)如果用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,烧瓶内压强迅速减小,外界大气压可将烧杯中的水压进烧瓶中形成喷泉,故答案为:打开夹子,用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,即发生喷泉.
点评:考查学生对元素化合物知识的熟悉程度.如题目1,学生综合题中信息,结合对物质性质的了解,猜测出一些物质C12、KC1O3等,再顺推、逆推和逐个验证,便可确定出全部答案.如果学生对题中的物质性质不熟悉,一下子被A、B、C、D、X、Y、Z乱了阵脚,便会乱猜一通.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-a kJ?mol-1
已知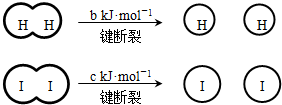 (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是( )
已知
 (a、b、c均大于零)
(a、b、c均大于零)下列说法不正确的是( )
| A、反应物的总能量高于生成物的总能量 | B、断开1mol H-H键和1mol I-I键所需能量大于断开2mol H-I键所需能量 | C、断开2mol H-I键所需能量约为(c+b+a)kJ | D、向密闭容器中加入2mol H2和2mol I2,充分反应后放出的热量小于2a kJ |

 已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
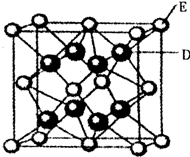 已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2P轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布和Ar原子相同,F的核电荷数是D和E的核电荷数之和.
已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2P轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布和Ar原子相同,F的核电荷数是D和E的核电荷数之和.