题目内容
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g)  2XY3(g) ΔH=—92.6KJ/mol
2XY3(g) ΔH=—92.6KJ/mol
实验测得反应在起始、达到平衡时的有关数据如下表所示:

下列叙述不正确的是
A.容器①、②中反应的平衡常数相等
B.达平衡时,两个容器中XY3的物质的量浓度均为2 mol/L
C.容器②中反应达到平衡时放出的热量为Q
D.若将容器①体积缩小为0.20 L,则达平衡时放出的热量大于23.15 kJ
C
【解析】
试题分析:由于反应是在相同温度下进行的,所以反应达到平衡时容器①、②中反应的平衡常数相等,正确;B.在相同温度下反应在容积相等的容器内进行。对于②来说,假设0.8mol的XY3是消耗X2、Y2反应产生的,则反应开始时X2、Y2的物质的量是1.0mol、3.0mol,与①相同,由于加入1mol的X2、3mol的Y2反应达到平衡时放出热量是23.15KJ,则反应消耗的X2的物质的量是23.15KJ÷ 92.6KJ/mol =0.25mol,则达到平衡时产生XY3的物质的量是0.50mol,其平衡浓度均为0.50mol÷0.25L=2 mol/L,正确;C.容器①、②的平衡状态等效。正反应是放热反应,逆反应是吸热反应,由于容器②中开始加入了0.8mol的 XY3,所以反应达到平衡时放出的热量小于23.15KJ,即小于Q,错误;D.若将容器①体积缩小为0.20 L,由于减小体积,也就增大的图像的压强,增大压强,平衡向气体体积减小的正反应方向移动,所以达平衡时放出的热量大于23.15 kJ,正确。
考点:考查可逆反应平衡状态的判断、物质的平衡浓度、反应热的多少及平衡常数大小比较的知识。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
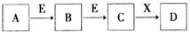 。下列推断不正确的是
。下列推断不正确的是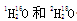 。下列有关说法正确的是
。下列有关说法正确的是
 cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是
cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是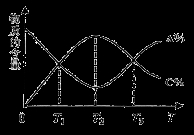
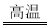 CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸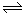 2SO3(g) △H=-197kJ/mol。在相同温度下,向密闭容器通入2mol SO2和1mol O2达平衡时,放热Q1;向另一相同体积的密闭容器中通入1mol SO2和0.5mol O2达平衡时,放出热量Q2,则下列关系式正确的是
2SO3(g) △H=-197kJ/mol。在相同温度下,向密闭容器通入2mol SO2和1mol O2达平衡时,放热Q1;向另一相同体积的密闭容器中通入1mol SO2和0.5mol O2达平衡时,放出热量Q2,则下列关系式正确的是