题目内容
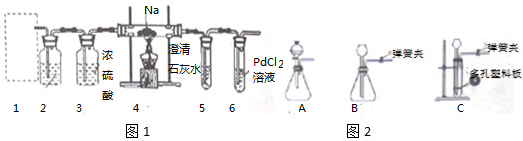
根据Mg能在CO2中燃烧,某兴趣小组推测Na应该也能在CO2中燃烧,且固体产物可能为C、Na2O和Na2CO3中的两种或三种.该小组用如图1装置进行了实验探究.已知PdCl2能被CO还原得到黑色的Pd.
回答下列问题:
(1)为了使反应随开随用,随关随停,上图虚线方框内应选用 装置(填图2中的字母代号),如何检验所选装置的气密性 .
(2)装置2中所盛试剂为 .
A.NaOH溶液 B.饱和NaHCO3溶液 C.饱和Na2CO3溶液 D.饱和NaCl溶液
(3)检测装置的气密性完好并装好药品后,在点燃酒精灯前应先进行装置1中的反应操作,待观察到 现象时,再点燃酒精灯,这步操作的目的是 .
(4)由实验现象和进一步的探究得出反应机理.
A.装置6中有黑色沉淀生成;
B.取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液;将溶液加水稀释配成250mL的溶液:
C.取25.00mL步骤B的溶液,滴加足量BaCl2溶液,将生成的白色沉淀过滤、洗涤、干燥,称量得固体质量为1.97g.
①步骤C中不溶物干燥前必须经过洗涤,如何检验该沉淀是否洗涤干净 .
②该探究得出钠与二氧化碳反应的化学方程式为 .

回答下列问题:
(1)为了使反应随开随用,随关随停,上图虚线方框内应选用
(2)装置2中所盛试剂为
A.NaOH溶液 B.饱和NaHCO3溶液 C.饱和Na2CO3溶液 D.饱和NaCl溶液
(3)检测装置的气密性完好并装好药品后,在点燃酒精灯前应先进行装置1中的反应操作,待观察到
(4)由实验现象和进一步的探究得出反应机理.
A.装置6中有黑色沉淀生成;
B.取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液;将溶液加水稀释配成250mL的溶液:
C.取25.00mL步骤B的溶液,滴加足量BaCl2溶液,将生成的白色沉淀过滤、洗涤、干燥,称量得固体质量为1.97g.
①步骤C中不溶物干燥前必须经过洗涤,如何检验该沉淀是否洗涤干净
②该探究得出钠与二氧化碳反应的化学方程式为
考点:性质实验方案的设计
专题:实验设计题
分析:(1)制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应该选用能够可以固、液药品分开的装置,根据装置特点确定检验所选装置的气密性的方法;
(2)由实验方案图可知装置b是除去二氧化碳中的HCl,应用饱和的碳酸氢钠溶液;
(3)由实验方案图可知,a为二氧化碳发生装置,d为二氧化碳与钠反应装置,加入d装置的二氧化碳应干燥,没有其其它,故装置b是除去二氧化碳其它中的HCl,应用饱和的碳酸氢钠溶液,c为干燥装置,吸收水蒸气.反应需要排尽装置内的空气,当e装置中产生白色沉淀,说明空气中的二氧化碳排尽,再加热d处的酒精灯发生反应;
(4)取最后一次洗涤液加入稀H2SO4,不出现浑浊说明沉淀洗涤干净;根据步骤A装置6中有黑色沉淀生成,可知钠与二氧化碳反应生成了一氧化碳;
步骤C中最终所得固体质量为1.97g为碳酸钡,说明反应生成碳酸钠,根据碳元素守恒可知碳酸钠的物质的量0.01mol,故23g固体物质中碳酸钠的物质的量为0.1mol,其质量10.6g,根据步骤B取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液,可知固体中有氧化钠,质量为:23-10.6=12.4g,物质的量为
=0.2mol;根据Na2O和Na2CO3物质的量之比为 0.2mol:0.1mol=2:1,利用元素守恒和电子守恒配平反应方程式为:6Na+4CO2
2Na2O+Na2CO3+3CO.
(2)由实验方案图可知装置b是除去二氧化碳中的HCl,应用饱和的碳酸氢钠溶液;
(3)由实验方案图可知,a为二氧化碳发生装置,d为二氧化碳与钠反应装置,加入d装置的二氧化碳应干燥,没有其其它,故装置b是除去二氧化碳其它中的HCl,应用饱和的碳酸氢钠溶液,c为干燥装置,吸收水蒸气.反应需要排尽装置内的空气,当e装置中产生白色沉淀,说明空气中的二氧化碳排尽,再加热d处的酒精灯发生反应;
(4)取最后一次洗涤液加入稀H2SO4,不出现浑浊说明沉淀洗涤干净;根据步骤A装置6中有黑色沉淀生成,可知钠与二氧化碳反应生成了一氧化碳;
步骤C中最终所得固体质量为1.97g为碳酸钡,说明反应生成碳酸钠,根据碳元素守恒可知碳酸钠的物质的量0.01mol,故23g固体物质中碳酸钠的物质的量为0.1mol,其质量10.6g,根据步骤B取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液,可知固体中有氧化钠,质量为:23-10.6=12.4g,物质的量为
| 12.4g |
| 62g/mol |
| ||
解答:
解:(1)制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应该选用能够可以固、液药品分开的装置,A中只能控制反应的速率,但不能控制反应的随时进行与停止;而C中当打开止水夹时,酸就和有孔塑料板上的石灰石反应生成气体,当关闭止水夹时,生成的气体就无法从导管中排出,从而使装置内的压强增大,把酸液挤到长颈漏斗中,使固液分离,故选C.检验所选装置的气密性的方法为:关闭弹簧夹,向长颈漏斗中加水,一定时间后静置液面保持不动,说明气密性良好,
故答案为:C;关闭弹簧夹,向长颈漏斗中加水,一定时间后静置液面保持不动,说明气密性良好;
(2)由实验方案图可知,a为二氧化碳发生装置,d为二氧化碳与钠反应装置,加入d装置的二氧化碳应干燥,没有其它,故装置b是除去二氧化碳中的HCl,应用饱和的碳酸氢钠溶液,
故答案为:B;
(3)由分析可知,反应需要排尽装置内的空气,当装置⑤中产生白色沉淀,说明空气中的二氧化碳排尽,再加热d处的酒精灯发生反应,
故答案为:装置⑤中产生白色沉淀;排尽装置内的空气;
(4)①检验该沉淀是否洗涤干净 取最后一次洗涤液加入稀H2SO4,不出现浑浊说明沉淀洗涤干净,
故答案为:取最后一次洗涤液加入稀H2SO4,不出现浑浊说明沉淀洗涤干净;
②根据步骤A装置6中有黑色沉淀生成,可知钠与二氧化碳反应生成了一氧化碳;步骤C中最终所得固体质量为1.97g为碳酸钡,说明反应生成碳酸钠,根据碳元素守恒可知,碳酸钠的物质的量=
=0.01mol,故23g固体物质中碳酸钠的物质的量为0.01mol×
=0.1mol,其质量=0.1mol×106g/mol=10.6g;
根据步骤B取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液,可知固体中有氧化钠,质量为:23-10.6=12.4g,物质的量为
=0.2mol;根据Na2O和Na2CO3物质的量之比为 0.2mol:0.1mol=2:1,利用元素守恒和电子守恒配平反应方程式为:6Na+4CO2
2Na2O+Na2CO3+3CO,
故答案为:6Na+4CO2
2Na2O+Na2CO3+3CO.
故答案为:C;关闭弹簧夹,向长颈漏斗中加水,一定时间后静置液面保持不动,说明气密性良好;
(2)由实验方案图可知,a为二氧化碳发生装置,d为二氧化碳与钠反应装置,加入d装置的二氧化碳应干燥,没有其它,故装置b是除去二氧化碳中的HCl,应用饱和的碳酸氢钠溶液,
故答案为:B;
(3)由分析可知,反应需要排尽装置内的空气,当装置⑤中产生白色沉淀,说明空气中的二氧化碳排尽,再加热d处的酒精灯发生反应,
故答案为:装置⑤中产生白色沉淀;排尽装置内的空气;
(4)①检验该沉淀是否洗涤干净 取最后一次洗涤液加入稀H2SO4,不出现浑浊说明沉淀洗涤干净,
故答案为:取最后一次洗涤液加入稀H2SO4,不出现浑浊说明沉淀洗涤干净;
②根据步骤A装置6中有黑色沉淀生成,可知钠与二氧化碳反应生成了一氧化碳;步骤C中最终所得固体质量为1.97g为碳酸钡,说明反应生成碳酸钠,根据碳元素守恒可知,碳酸钠的物质的量=
| 1.97g |
| 197g/mol |
| 250 |
| 25 |
根据步骤B取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液,可知固体中有氧化钠,质量为:23-10.6=12.4g,物质的量为
| 12.4g |
| 62g/mol |
| ||
故答案为:6Na+4CO2
| ||
点评:本题考查物质组成与探究,涉及对实验方案的理解、实验基本操作、化学计算与数据处理等,确定生成物的成分以发生的反应是难度,也是易错点,题目难度较大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
现代家居装修材料中,普遍存在着甲醛、苯及苯的同系物等有毒物质,如果不注意处理就会对人体产生极大的危害.按照有机物的分类,甲醛属于醛.下列各项对有机物的分类方法与此方法相同的是( )


| A、①② | B、②③ | C、②④ | D、①④ |
下列反应中,属于加成反应的是( )
A、CH3Cl+Cl2
| |||
B、CH2=CH2+H2O
| |||
C、2CH3CH2OH+O2
| |||
D、 |