��Ŀ����
8����ϩ��һ���¶ȡ�ѹǿ����ˮ��Ӧ�Ʊ��Ҵ��Ĺ������£���ϩ$\stackrel{ŨH_{2}SO_{4}}{��}$C2H5OSO3H$��_{��}^{H_{2}O}$H2SO4+C2H5OH�����й�˵���д�����ǣ�������| A�� | ��Ӧ���Ǽӳɷ�Ӧ����Ӧ����ȡ����Ӧ | |
| B�� | ��Ӧ�����п��ܻ�������Ⱦ������ | |
| C�� | C2H5OSO3H���Ҵ�������ʹ����KMnO4��Һ��ɫ | |
| D�� | ����ʹ��Ũ���ᣬ��ϩ������ˮ��Ӧ������Ӧ���ʷdz��� |
���� A����ϩ�к�̼̼˫������Ũ���ᷢ���ӳɷ�Ӧ����C2H5OSO3H����ˮ�������Ҵ���
B��Ũ���������ˮ�ԣ���C����������ԭ��Ӧ���ɶ�������
C���Ҵ��ܱ��������������
D����ϩ��ˮ�����ӳɷ�Ӧ�����Ҵ�����Ӧ������
��� �⣺A����ϩ�к�̼̼˫������Ũ���ᷢ���ӳɷ�Ӧ����C2H5OSO3H����ˮ�������Ҵ�����Ӧ���Ǽӳɷ�Ӧ����Ӧ����ȡ����Ӧ����A��ȷ��
B��Ũ���������ˮ�ԣ���C����������ԭ��Ӧ���ɶ���������Ӧ�����п��ܻ�������Ⱦ�����壬��B��ȷ��
C���Ҵ��ܱ�����������������Ҵ���ʹ����KMnO4��Һ��ɫ����C����
D����ϩ��ˮ�����ӳɷ�Ӧ�����Ҵ�����Ӧ��������Ӧʹ��Ũ���ᣬ��D��ȷ��
��ѡC��
���� ���⿼���л���ĺϳɼ��ṹ�����ʣ�Ϊ��Ƶ���㣬�������ʵ����ʡ��л���ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���

��ϰ��ϵ�д�
 ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
ͬ������ϵ�д�
�����Ŀ
18����ѧ����ᡢ����������������أ�����˵������ȷ���ǣ�������
| A�� | �������������������β���Ĵ�����������������߿������� | |
| B�� | ���ٻ�ʯȼ�ϵ�ʹ�ã������ڽ��Ϳ�����PM2.5�ĺ��� | |
| C�� | ʳƷ��װ���г�����С������ʯ�ң�Ŀ���Ƿ�ֹʳƷ�������� | |
| D�� | ҽ�þƾ����õ�����ֲ��;������Ƴɣ�Ũ��ͨ����75% |
19��X��Y��Z��W��ԭ������������������ֶ���������Ԫ�أ���֪Z���������������۵Ĵ�����Ϊ4��Y���γ����ֳ�����Һ���Ԫ������M��Q������M�����������������ʣ�X���γɶ��ֵ��ʣ����������ֵ���Ӳ�Ȳ��켫������˵���д�����ǣ�������
| A�� | ����������Ӧˮ��������ԣ�W��Z��X | |
| B�� | ������Q��ǿ������ | |
| C�� | Z��X�������γ����ֳ��������������� | |
| D�� | ����Ԫ�صij���������X�ĵ��ʵķе���� |
3������������Ȼ���й㷺���ڣ�����ѭ����ϵ���£�
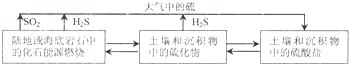
��1����֪��
2H2S��g��+3O2��g���T2SO2��g��+2H2O��g����H=-1036.46kj��mol-1
S��s��+O2��g���TSO2��g����H=-297.04kJ��mol-1
д��H2S��g����O2��g����Ӧ����S��s����H2O��g�����Ȼ�ѧ����ʽ2H2S��g��+O2��g��=2S��g��+2H2O��g����H=-442.38kJ��mol-1��
��2����Ȼ��ر���ԭ��ͭ�����ᆳ�������������ú���CuSO4��Һ���������������������ܵ�ZnS������ת��Ϊͭ����CuS���������ӷ���ʽ���ӳ����ܽ�ƽ��ĽǶȱ�ʾ��ZnSת��ΪCuS�Ĺ���ZnS��S��+Cu2+��aq��?Zn2+��aq��+CuS��S����
��3��ij����FeSO4��Һ�к���������SnSO4��Ϊ�õ������������������壨FeSO4•xH2O����������Һ��ͨ��H2S���������ͣ�Ȼ���������ữ��Ph=2�����˺�������Һ����Ũ������ȴ�ᾧ������ϴ�ӣ��õ������������壮�������ϣ��õ�������ʵ��й��������±���
��ͨ��H2S���������͵�Ŀ���ǽ���Һ�е�Sn2+ת��ΪSnS����ȥ���������ữ��pH=2��Ŀ���Ƿ�ֹFe2+ת��ΪFeS������
����SnS��FeS�������Һ�У���c��Sn2+��=1.0��10-9mol•L-1����c��Fe2+��=6.3��10-2mol•L-1��
��4��SO2�Ǵ�����Ⱦ�����KMnO4�����������ʹȼúβ���е�SO2��Ӧ����MnSO4����Ӧ�����ӷ���ʽ��2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+��SO2���������������Ʊ�����ԭ�����ᣬ��Ӧ���з�����Ӧ�Ļ�ѧ����ʽ��SO2+xI2+2H2O=H2SO4+2HIx��
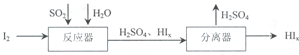

��1����֪��
2H2S��g��+3O2��g���T2SO2��g��+2H2O��g����H=-1036.46kj��mol-1
S��s��+O2��g���TSO2��g����H=-297.04kJ��mol-1
д��H2S��g����O2��g����Ӧ����S��s����H2O��g�����Ȼ�ѧ����ʽ2H2S��g��+O2��g��=2S��g��+2H2O��g����H=-442.38kJ��mol-1��
��2����Ȼ��ر���ԭ��ͭ�����ᆳ�������������ú���CuSO4��Һ���������������������ܵ�ZnS������ת��Ϊͭ����CuS���������ӷ���ʽ���ӳ����ܽ�ƽ��ĽǶȱ�ʾ��ZnSת��ΪCuS�Ĺ���ZnS��S��+Cu2+��aq��?Zn2+��aq��+CuS��S����
��3��ij����FeSO4��Һ�к���������SnSO4��Ϊ�õ������������������壨FeSO4•xH2O����������Һ��ͨ��H2S���������ͣ�Ȼ���������ữ��Ph=2�����˺�������Һ����Ũ������ȴ�ᾧ������ϴ�ӣ��õ������������壮�������ϣ��õ�������ʵ��й��������±���
| 25�� | ����H2S��Һ | FeS | SnS | |
| pH | 3.9 | 3.0����ʼ���� | 5.5��������ȫ�� | 1.6��������ȫ�� |
| Ksp | 6.3��10-18 | 1.0��10-25 | ||
����SnS��FeS�������Һ�У���c��Sn2+��=1.0��10-9mol•L-1����c��Fe2+��=6.3��10-2mol•L-1��
��4��SO2�Ǵ�����Ⱦ�����KMnO4�����������ʹȼúβ���е�SO2��Ӧ����MnSO4����Ӧ�����ӷ���ʽ��2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+��SO2���������������Ʊ�����ԭ�����ᣬ��Ӧ���з�����Ӧ�Ļ�ѧ����ʽ��SO2+xI2+2H2O=H2SO4+2HIx��

13��������������ΪSiO2��Fe2O3�ȣ�Ϊԭ��ұ�������������£�������Һb�ʼ��ԣ�������˵������ȷ���ǣ�������


| A�� | ��Ӧ������ӷ���ʽΪ2OH-+Al2O3�T2AlO2-+H2O | |
| B�� | ����a�����ݰ�����ͨ�����CO2�����ˡ�ϴ�ӡ����� | |
| C�� | ����bΪ�������״̬��Al2O3����CO��ԭAl2O3 | |
| D�� | ����b���պ�������Ӧ�����ڹ�ҵ��ұ����Ӧ�Ľ��� |
20���Դ�1902��¹���ѧ�ҹ����о����ϳɰ��ķ������������Ĺ̶�������о�����˲��ϵķ�չ��
��1���±��о��˲�ͬ�¶��´����̵��IJ���ƽ�ⳣ��Kֵ��
�ٷ������ݿ�֪�������̵���Ӧ�������ȣ�����ȡ����ȡ�����Ӧ��
��2260��ʱ����2L�ܱ������г���0.3molN2��0.3molO2��ģ������̵���Ӧ���ﵽƽ��ʱ��N2��ת������33.3%�����������λ��Ч���֣���
��2����ҵ�̵�����Ҫ��ʽ�ǣ�N2 ��g��+3H2 ��g��=2NH3 ��g����H��0����ͼ�ǵ���Ӧ���а�n��N2����n��H2��=1��3 Ͷ�Ϻ���200�桢400�桢600���£���Ӧ�ﵽƽ��ʱ���������NH3�����ʵ���������ѹǿ�ı仯���ߣ�
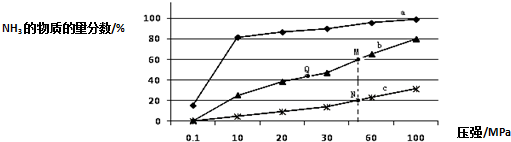
������a��Ӧ���¶���200�森
�ڹ��ڹ�ҵ�ϳɰ��ķ�Ӧ������������ȷ����A������ĸ����
A��ͼ��M��N��Q��ƽ�ⳣ��K�Ĵ�С��ϵ��K��M��=K��Q����K��N��
B����ҵ�ϳɰ�֮�����Լ������������Ϊ���������������߷�Ӧ�Ļ��
C����ͬѹǿ�£�Ͷ����ͬ���ﵽƽ������ʱ���ϵΪc��b��a
��N��ʱc��NH3��=0.2mol/L��N��Ļ�ѧƽ�ⳣ��K=0.93�����������λС������
��3���ϳɰ�ԭ�����е�����������Ȼ������Ҫ�ɷ�ΪCH4���ڸ��¡�������������ˮ������Ӧ�Ƶã���Ӧ��ÿ����2mol CO2����316kJ�������÷�Ӧ���Ȼ�ѧ����ʽ��CH4��g��+2H2O��g��=CO2��g��+4H2��g����H=+158kJ/mol���÷����Ƶõ�ԭ��������Ҫ������CO2������K2CO3��Һ���գ��÷�Ӧ�����ӷ���ʽ��CO32-+CO2+H2O=2HCO3-��
��4���ϳɰ���ҵ�к�����ˮ�Ĵ�������֮һ�ǵ绯ѧ���������������ļ��Է�ˮͨ����ϵͳ���������ϰ��������ɵ������ѳ��������ĵ缫��ӦʽΪ2NH3-6e-+6OH-=N2+6H2O��
��1���±��о��˲�ͬ�¶��´����̵��IJ���ƽ�ⳣ��Kֵ��
| ��Ӧ | �����̵�N2��g��+O2��g��?2NO��g�� | |
| �¶�/�� | 27 | 2260 |
| K | 3.84��10-31 | 1 |
��2260��ʱ����2L�ܱ������г���0.3molN2��0.3molO2��ģ������̵���Ӧ���ﵽƽ��ʱ��N2��ת������33.3%�����������λ��Ч���֣���
��2����ҵ�̵�����Ҫ��ʽ�ǣ�N2 ��g��+3H2 ��g��=2NH3 ��g����H��0����ͼ�ǵ���Ӧ���а�n��N2����n��H2��=1��3 Ͷ�Ϻ���200�桢400�桢600���£���Ӧ�ﵽƽ��ʱ���������NH3�����ʵ���������ѹǿ�ı仯���ߣ�

������a��Ӧ���¶���200�森
�ڹ��ڹ�ҵ�ϳɰ��ķ�Ӧ������������ȷ����A������ĸ����
A��ͼ��M��N��Q��ƽ�ⳣ��K�Ĵ�С��ϵ��K��M��=K��Q����K��N��
B����ҵ�ϳɰ�֮�����Լ������������Ϊ���������������߷�Ӧ�Ļ��
C����ͬѹǿ�£�Ͷ����ͬ���ﵽƽ������ʱ���ϵΪc��b��a
��N��ʱc��NH3��=0.2mol/L��N��Ļ�ѧƽ�ⳣ��K=0.93�����������λС������
��3���ϳɰ�ԭ�����е�����������Ȼ������Ҫ�ɷ�ΪCH4���ڸ��¡�������������ˮ������Ӧ�Ƶã���Ӧ��ÿ����2mol CO2����316kJ�������÷�Ӧ���Ȼ�ѧ����ʽ��CH4��g��+2H2O��g��=CO2��g��+4H2��g����H=+158kJ/mol���÷����Ƶõ�ԭ��������Ҫ������CO2������K2CO3��Һ���գ��÷�Ӧ�����ӷ���ʽ��CO32-+CO2+H2O=2HCO3-��
��4���ϳɰ���ҵ�к�����ˮ�Ĵ�������֮һ�ǵ绯ѧ���������������ļ��Է�ˮͨ����ϵͳ���������ϰ��������ɵ������ѳ��������ĵ缫��ӦʽΪ2NH3-6e-+6OH-=N2+6H2O��
17�������й����ӷ���ʽ��д�����ӹ���˵����ȷ���ǣ�������
| A�� | ��0.1 mol/L Na2CO3��Һ�У�Al3+��NH4+��SO42-��NO3-һ���ܴ������� | |
| B�� | �����£�$\frac{{K}_{W}}{c��{H}^{+}��}$=0.1 mol/L����Һ�У���������һ���ܴ������棺K+��Cl-��Fe2+��NO3- | |
| C�� | ��ϴ��¯ʱ���ô�����Һ���ݵ���Ҫԭ��CaSO4��s��+CO32-��aq��?SO42-��aq��+CaCO3��s�� | |
| D�� | ��Al2��SO4��3��Һ�м�������Ba��OH��2��Һ��Ba2++SO42-+Al3++3OH-�TBaSO4��+Al��OH��3�� |
18������ʵ���������ʵ�����������Ӱ����ǣ�������
| A�� | ������ˮʪ��pH��ֽ��ⶨ��������Һ��pH | |
| B�� | �ⶨ�кͷ�Ӧ�ķ�Ӧ��ʱ��������Һ������������Һ�� | |
| C�� | ������к͵ζ����ⶨδ֪Ũ�ȵļ�Һʱ������ƿ�м���2-3mL��̪��Һ��ָʾ�� | |
| D�� | �ڵ�����Һ�м���ϡ�������һ��ʱ����ٵμ�������Һ������۵�ˮ����� |
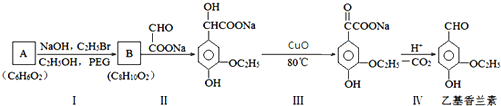
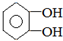 ��
��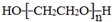 ����PEG��ƽ����Է�������Ϊ17618������ƽ���ۺ϶�ԼΪ400��
����PEG��ƽ����Է�������Ϊ17618������ƽ���ۺ϶�ԼΪ400��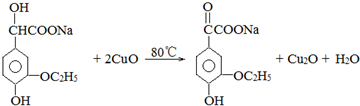 ��
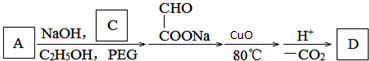
��
 ��
��