题目内容
常温下,pH都等于9的NaOH溶液和CH3COONa两种溶液中,若由水电离产生OH- 浓度分别为a mol/L和b mol/L,则a和b的关系是
| A.a>b | B.a=10-4b | C.b=10-4a | D.a=b |
B
试题分析:根据H2O
 H++OH-,从影响水的电离平衡移动的角度分析,NaOH抑制水的电离,CH3COONa促进水的电离,据此可以解答。pH=9的NaOH溶液,由NaOH电离产生的c(OH-)=10-5mol/L,则由水电离产生的c(OH-)=c(H+)=
H++OH-,从影响水的电离平衡移动的角度分析,NaOH抑制水的电离,CH3COONa促进水的电离,据此可以解答。pH=9的NaOH溶液,由NaOH电离产生的c(OH-)=10-5mol/L,则由水电离产生的c(OH-)=c(H+)=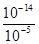 mol/L=10-9mol/L,即a=10-9mol/L;pH=9的CH3COONa溶液促进水的电离,OH-全部由水电离产生,c(OH-)=10-5mol/L,即b=c(OH-)=10-5mol/L,所以a:b=10-9mol/L:10-5mol/L=10-4,即a=10-4b,答案选B。
mol/L=10-9mol/L,即a=10-9mol/L;pH=9的CH3COONa溶液促进水的电离,OH-全部由水电离产生,c(OH-)=10-5mol/L,即b=c(OH-)=10-5mol/L,所以a:b=10-9mol/L:10-5mol/L=10-4,即a=10-4b,答案选B。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
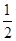 N2O4(g)=
N2O4(g)=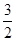 N2(g)+2H2O(g) ΔH="-1076.7" kJ·mol-1
N2(g)+2H2O(g) ΔH="-1076.7" kJ·mol-1