题目内容
18.下列反应中,属于吸热反应的是( )| A. | 锌与硫酸反应制取氢气 | B. | NaOH与HCl的反应 | ||
| C. | 高温煅烧石灰石 | D. | 铝与稀盐酸 |
分析 根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应、绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:A、金属与酸的反应为放热反应,故A错误;
B、酸碱中和为放热反应,故B错误;
C、绝大多数的分解反应为吸热反应,故高温煅烧石灰石使其分解为吸热反应,故C正确;
D、金属与酸的反应为放热反应,故铝和盐酸的反应为放热反应,故D错误.
故选C.
点评 本题考查吸热反应,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
8.某温度下,在一固定容积的容器中进行反应SO3(g)+NO(g)?NO2(g)+SO2(g),下列情况一定能说明已经达到化学反应限度的是( )
| A. | 体系总压强不再随时间而改变 | B. | 体系总质量不再随时间而改变 | ||
| C. | NO(g)和NO2(g)的生成速率相同 | D. | SO3(g)和NO(g)的浓度比为1:1 |
13.下列各组粒子中粒子半径由小到大的是( )
| A. | O2- Na+Mg2+Al3+ | B. | O P S Cl | ||
| C. | A l3+Mg2+ Na+ F- | D. | K+ Mg2+ Al3+ H+ |
3.1999年是人造元素丰收年,一年间得到了核电荷数分别为114、116和118三种新元素,已知核电荷数为118的新元素的一种原子的质量数为293,则该原子中子与电子数之差为( )
| A. | 0 | B. | 57 | C. | 118 | D. | 175 |
10.下列表达式错误的是( )
| A. | 甲烷的电子式: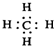 | |
| B. | 氮原子的L层电子的电子排布图: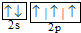 | |
| C. | 碳-12原子:${\;}_{6}^{12}$C | |
| D. | S2-的核外电子排布式:1s22s22p63s23p4 |
7.x、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知( )
| A. | x的原子半径大于y的原子半径 | |
| B. | x的第一电离能小于y 的第一电离能 | |
| C. | x阴离子的半径小于y阳离子的半径 | |
| D. | x的电负性大于y的电负性 |
8.下列化学用语使用正确的是( )
| A. | NH4Cl的电子式: | |
| B. | 用电子式表示氯化氢分子的形成过程: | |
| C. | 氧化钠的电子式: | |
| D. | R2+离子核外有a个电子,b个中子,R原子表示为:${\;}_{a+2}^{a+b+2}$R |



