题目内容
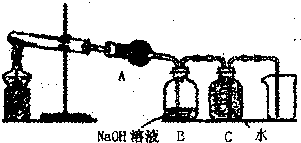
将一定量由碳、氢、氧三种元素组成的有机化合物A的蒸气与3.2g氧气混合点燃,再将生成的气体依次通过①盛有浓硫酸的洗气瓶 ②灼热的氧化铜 ③饱和石灰水(设每个装置中的反应物均过量).经测定①中增重3.60g ②中减重1.60g ③中增重8.80g.A蒸气的密度为3.393g?L-1(已换算成标准状况).又测知该蒸气既能与碳酸钠溶液反应又能与金属钠反应,且均有气体生成,但分别得到的气体在相同条件下体积不同,试求该有机物的分子式,并写出其可能的结构简式.
考点:有机物实验式和分子式的确定
专题:烃及其衍生物的燃烧规律
分析:A蒸气的密度是3.393g?L-1,则A的相对分子质量为3.393g/L×22.4L/mol=76,该有机物既能与碳酸钠溶液反应又能与金属钠反应,且均有气体生成,故该有机物一定含有-COOH,可能含有-OH,但得到的气体在相同条件下体积不同,故该有机物含有-COOH、-OH,故剩余基团的式量为76-45-17=14,故剩余基团的组成为CH2,据此解答.
解答:
解:A蒸气的密度是3.393g?L-1,则A的相对分子质量为3.393g/L×22.4L/mol=76,该有机物既能与碳酸钠溶液反应又能与金属钠反应,且均有气体生成,故该有机物一定含有-COOH,可能含有-OH,但得到的气体在相同条件下体积不同,故该有机物含有-COOH、-OH,故剩余基团的式量为76-45-17=14,故剩余基团的组成为CH2,故有机物A的结构简式为HOCH2COOH,分子式为C2H4O3,
答:有机物A的分子式为C2H4O3,结构简式为HOCH2COOH.
答:有机物A的分子式为C2H4O3,结构简式为HOCH2COOH.
点评:本题考查有机物分子式的确定,注意利用残余法解答,判断有机物含有的官能团是关键,注意题目中告诉的氧气、浓硫酸增重、饱和石灰水增重为干扰信息,该数据无法利用.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如装置①.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列叙述不正确的是( )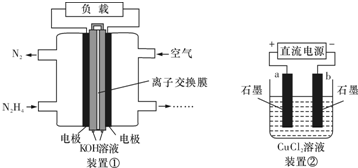

| A、该燃料电池负极发生的电极反应为:N2H4+4OH--4e-═N2+4H2O |
| B、用该燃料电池作为装置②的直流电源,产生1 mol Cl2至少需要通入0.5 mol N2H4 |
| C、该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
| D、该燃料电池中,电子从右侧电极经过外电路流向左侧电极,溶液中OH-则迁移到左侧 |