题目内容
15.某元素的原子核外电子排布中,K电子层和L电子层电子数之和等于M电子层和N电子层电子数之和,则该元素的核电荷数为( )| A. | 30 | B. | 20 | C. | 12 | D. | 17 |
分析 由于该元素原子含有M、N电子层,故K层、L层已经排满,K电子层和L电子层的电子数之和为10,所以M电子层和N电子层的电子数之和也为10.电中性原子核电荷数=质子数=核外电子数,以此解答该题.
解答 解:由于该元素原子含有M、N电子层,故K层、L层已经排满,K电子层和L电子层的电子数之和为10,所以M电子层和N电子层的电子数之和也为10,故该元素原子核外电子数为10+10=20,所以该元素核电荷数为20.
故选B.
点评 本题考查核外电子排布规律等,为高频考点,侧重于学生的分析能力的考查,比较基础,掌握核外电子排布规律并能灵活运用.

练习册系列答案
相关题目
5.对H2O的电离平衡不产生影响的粒子是( )
| A. | HCl | B. | Fe3+ | C. | 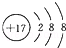 | D. | CH3COO- |
6.下列说法不正确的是( )
| A. | 量取10.08 mL 0.1 mol•L-1 NaHCO3溶液用碱式滴定管量取 | |
| B. | 为测定新制氯水的 pH,用玻璃棒蘸取液体滴在 pH 试纸上,与标准比色卡对照即可 | |
| C. | 探究催化剂对 H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL 5%H2O2和1mL H2O,向另一支试管中加入2mL 5%H2O2和1mL FeCl3溶液,观察并比较实验现象 | |
| D. | 已知 4H++4I-+O2=2I2+2H2O,为了利用该反应探究反应速率与温度的关系,所用试剂除1 mol•L-1 KI 溶液、0.1 mol•L-1 稀硫酸外,还需要用到淀粉溶液 |
3.如表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -2 |
| A. | X、Y分别与W形成的化合物都具有两性 | |
| B. | Z、W在同一主族 | |
| C. | 气态氢化物的稳定性为H2W<H2Z | |
| D. | X和Y对应的氢氧化物的碱性强弱比较:X(OH)2<Y(OH)3 |
10.下列有关化学用语正确的是( )
①乙烯的最简式:C2H4
②乙醇的结构简式:C2H6O
③乙烷的结构式:CH3CH3
④四氯化碳的电子式:
⑤乙醛的结构简式:CH3COH.
①乙烯的最简式:C2H4
②乙醇的结构简式:C2H6O
③乙烷的结构式:CH3CH3
④四氯化碳的电子式:

⑤乙醛的结构简式:CH3COH.
| A. | 全对 | B. | 全错 | C. | ③④ | D. | ①⑤ |
20.一定温度下,下列溶液的离子浓度关系式正确的是( )
| A. | pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol•L-1 | |
| B. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a>b+1 | |
| C. | pH=9的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):①>③>② | |
| D. | pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-) |
7.某温度下,关于浓度相等的盐酸和醋酸溶液,下列说法正确的是( )
| A. | pH HCl>CH3COOH | |
| B. | c(Cl-)=c(CH3COO-) | |
| C. | 等体积的盐酸和醋酸溶液分别与足量的Zn完全反应,盐酸产生的H2多 | |
| D. | 用同浓度的NaOH溶液分别与等体积的盐酸和醋酸溶液恰好反应完全,消耗的NaOH溶液体积一样多 |
4.适当可以加热,只用一种试剂就可以鉴别的物质组是( )
| A. | NaCl、KNO3、AlCl3、Fe(NO3)3 | B. | Fe、FeO、CuO、FeS、CuS、MnO2 | ||
| C. | MgCl2、FeCl2、KCl、AlCl3、NH4Cl | D. | K2CO3、NaI、Na2CO3、NaCl、Na2SO4 |
15.有关下列物质分子结构特征描述正确的是( )
| A. | 乙烯容易与溴的四氯化碳溶液发生反应,且1mol乙烯完全加成消耗1mol溴单质,证明乙烯分子里含有一个碳碳双键 | |
| B. | 苯分子的结构中存在碳碳单键和碳碳双键交替出现的结构 | |
| C. | 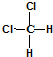 和 和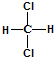 属于同一种物质,不能用来解释甲烷是一种正四面体结构 属于同一种物质,不能用来解释甲烷是一种正四面体结构 | |
| D. | 1mol CH3CH2OH与Na完全反应只生成0.5mol H2,不能说明乙醇分子中有一个氢原子与其它氢原子不同 |