题目内容
19.水热法制备Fe2O3纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O62-+2H2O,关于该反应下列说法正确的是( )| A. | H2O和S4O62-都是还原产物 | |
| B. | 1mol Fe2+参加反应时,转移2mol电子 | |
| C. | Fe2+、S2O32-都是还原剂 | |
| D. | x=2 |
分析 3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O62-+2H2O中,由电荷守恒可知,x=4,Fe、S元素的化合价升高,O元素的化合价降低,以此来解答.
解答 解:A.S元素的化合价升高,S4O62-是氧化产物,故A错误;
B.由O元素的化合价变化可知,该反应转移4mol电子,此时2molFe2+失去电子,则1mol Fe2+参加反应时,转移2mol电子,故B正确;
C.$\frac{2}{3}$的Fe2+及S2O32-是还原剂,故C错误;
D.由电荷守恒可知,x=4,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化、电子及电荷守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法应用,题目难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案
相关题目
10.下列说法中,正确的是( )
| A. | 气体的摩尔体积为22.4 L•mol-12 | |
| B. | 1 mol H2的质量是2 g,它所占的体积是22.4 L | |
| C. | 在标准状况下,1 mol任何气体所占的体积都为22.4 L•mol-1 | |
| D. | 在标准状况下,1 mol任何气体所占的体积都约为22.4 L |
7.下式表示一种有机物的结构,关于它的性质叙述中不正确的是( )
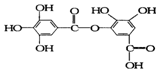

| A. | 它能与纯碱溶液反应 | |
| B. | 它可以水解,水解生成的有机产物有二种 | |
| C. | 1 mol该有机物最多能和8 mol NaOH反应 | |
| D. | 该有机物能发生取代反应 |
14.下列关于有机物的说法不正确的是( )
| A. | C3H2Cl6有四种同分异构体 | |
| B. | 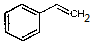 中所有原子可能共平面 中所有原子可能共平面 | |
| C. | 乙醇被酸性KMnO4溶液充分氧化的化学方程式为5CH3CH2OH+2KMnO4+3H2SO4→5CH3CHO+K2SO4+2MnSO4+8H2O | |
| D. | -C3H7和-C2H5O各取代苯分子中的一个氢原子形成的二元取代物的同分异构体有24种 |
4.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A. | 沉淀溶解后,将会生成深蓝色的配合离子[Cu(NH3)4]2+ | |
| B. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| C. | 向反应后的溶液加入乙醇,溶液不会有变化,因为[Cu(NH3)4]2+不会与乙醇发生反应 | |
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
11.在容积相同的①、②、③三个烧瓶中分别充满NH3、HCl和NO2气体,当把烧瓶倒扣到水中且水与气体充分反应后,所得溶液的物质的量浓度的关系是( )
| A. | ①=②=③ | B. | ①>②>③ | C. | ①=②>③ | D. | ①=②<③ |
8.化学与人类生活、社会可持续发展密切相关.下列有关叙述中不正确的是( )
| A. | 回收废弃塑料制成燃油来替代汽油、柴油,可减轻环境污染和节约化石能源 | |
| B. | 火药是我国古代四大发明之一,配方为“一硫二硝三木炭”,其中的“硝”是指硝酸 | |
| C. | 高压钠灯发出的黄光射程远、透雾能力强,常用作路灯 | |
| D. | 黑色金属材料通常包括铁、铬、锰以及它们的合金,是应用非常广泛的金属材料 |
9.以下有机物同分异构体数目判断中不正确的是( )
| A. | 立方烷( 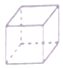 )的六氨基(-NH2)取代物有3种 )的六氨基(-NH2)取代物有3种 | |
| B. | C3H7ClO(有羟基)的同分异构体数目有5种 | |
| C. | 甲苯与氢气充分加成后的一溴代物有4种 | |
| D. | 分子式为C5H10O2的有机物中能与NaOH溶液反应的有13种 |