题目内容
请按要求填空
(1)检验稀盐酸中是否含有SO42-离子,加入的试剂为 (填化学式)溶液.
(2)除去NaCl固体中混有的少量KNO3,所进行的实验操作依次为: 、蒸发、结晶、过滤.
(3)用已准确称量的Na2CO3固体配制0.10mol/L Na2CO3溶液100mL,所需要的仪器除烧杯、量筒、玻璃棒和胶头滴管外,还需要的仪器为 .
(1)检验稀盐酸中是否含有SO42-离子,加入的试剂为
(2)除去NaCl固体中混有的少量KNO3,所进行的实验操作依次为:
(3)用已准确称量的Na2CO3固体配制0.10mol/L Na2CO3溶液100mL,所需要的仪器除烧杯、量筒、玻璃棒和胶头滴管外,还需要的仪器为
考点:常见阴离子的检验,溶液的配制,物质的分离、提纯的基本方法选择与应用
专题:物质检验鉴别题,化学实验基本操作
分析:(1)检验硫酸根离子,需要选用钡离子,可以选用氯化钡溶液;
(2)氯化钠的溶解度受温度影响减小,硝酸钾后温度影响较大,可以通过重结晶法分离氯化钠和硝酸钾;
(3)根据配制一定物质的量浓度的溶液方法选用仪器,判断还缺少的仪器.
(2)氯化钠的溶解度受温度影响减小,硝酸钾后温度影响较大,可以通过重结晶法分离氯化钠和硝酸钾;
(3)根据配制一定物质的量浓度的溶液方法选用仪器,判断还缺少的仪器.
解答:
解:(1)检验稀盐酸中是否含有SO42-离子,可以使用BaCl2溶液进行检验,故答案为:BaCl2;
(2)除去NaCl固体中混有的少量KNO3,可以使用重结晶反应,先将固体溶解,然后通过蒸发、结晶、过滤等操作分离,得到纯净的硝酸钾固体,
故答案为:溶解;
(3)用已准确称量的Na2CO3固体配制0.10mol/L Na2CO3溶液100mL,所需要的仪器除烧杯、量筒、玻璃棒和胶头滴管外,配制100mL溶液,选100mL容量瓶来配制,
故答案为:100 mL容量瓶.
(2)除去NaCl固体中混有的少量KNO3,可以使用重结晶反应,先将固体溶解,然后通过蒸发、结晶、过滤等操作分离,得到纯净的硝酸钾固体,
故答案为:溶解;
(3)用已准确称量的Na2CO3固体配制0.10mol/L Na2CO3溶液100mL,所需要的仪器除烧杯、量筒、玻璃棒和胶头滴管外,配制100mL溶液,选100mL容量瓶来配制,
故答案为:100 mL容量瓶.
点评:本题考查了常见阴离子检验、一定浓度的溶液配制、物质的分离与提纯,题目难度中等,注意掌握常见离子的性质及检验方法,明确配制一定物质的量浓度的溶液步骤及选用仪器方法,还要熟悉物质分离与提纯方法.

练习册系列答案
相关题目
常温下,0.1mol/L某一元酸(HA)溶液中
=1×10-8,下列叙述正确的是( )
| c(OH-) |
| c(H+) |
| A、溶液中水电离出的c(H+)=10-10mol/L |
| B、溶液中c(H+)+c(A-)=0.1mol/L |
| C、溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大 |
| D、与0.05mol/LNaOH溶液等体积混合后所得溶液中离子浓度大小关系为 c(A-)>c(Na+)>c(OH-)>c(H+) |
对于电解质溶液,下列说法不正确的是( )
| A、常温下,pH=2的氯水中:c(Cl-)+c(ClO-)+c(OH-)=0.01mol/L |
| B、用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+═Cu2++2H2O |
| C、MgCO3可以除去MgCl2酸性溶液中的Fe3+ |
| D、在pH=1的溶液中,NH4+、K+、ClO-、Cl-可以大量共存 |
 如图,将两烧杯用导线相连,Pt、Cu、Zn、C分别为四个电极,当闭合开关后,以下叙述正确的是( )
如图,将两烧杯用导线相连,Pt、Cu、Zn、C分别为四个电极,当闭合开关后,以下叙述正确的是( )| A、Cu极附近OH-浓度增大 |
| B、Cu极为原电池负极 |
| C、电子流向是由C极流向Pt极 |
| D、当C极上有4mol电子转移时,Pt极上有1mol O2生成 |
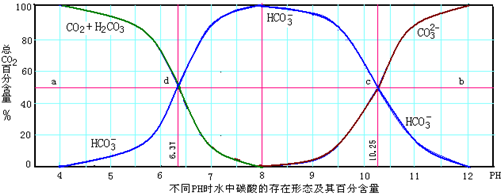
 已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+;△H>0
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+;△H>0