题目内容
2.如图所示的甲、乙两个装置中(常温),胶头滴管中吸入某种液体,圆底烧瓶中充入(或放入)另一种物质,挤压胶头滴管中液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )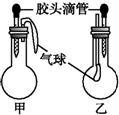 | 甲 | 乙 | |||
| 滴管中 | 烧瓶中 | 滴管中 | 烧瓶中 | ||
| A | 水 | 过氧化钠 | 饱和碳酸氢钠溶液 | CO2 | |
| B | NaOH溶液 | 铝 | 硫酸钠溶液 | CO2 | |
| C | NaOH溶液 | 碳酸氢钠 | 澄清石灰水 | 碳酸氢钠 | |
| D | 稀盐酸 | 碳酸氢钠 | NaOH溶液 | CO2 | |
| A. | A | B. | B | C. | C | D. | D |
分析 甲装置气球膨大原因是烧瓶内有气体生成或者温度升高,使烧瓶内的压强大于外界压强;乙装置气球膨大原因是烧瓶内的气体参加反应或者温度降低,使烧瓶内的压强小于外界压强,结合物质的性质结合发生的反应结合原理来解答.
解答 解:A.甲中水和过氧化钠之间反应生成氧气,使容器内压强大于大气压,所以气球变大;乙中二氧化碳不溶于饱和碳酸氢钠钠溶液,所以容器内气体压强不变,气球不变化,故A错误;
B.甲中过氧化钠和水反应生成氧气,使容器内压强大于大气压,所以气球变大;乙中二氧化碳和硫酸钠不反应,使容器内压强不变,所以气球不变,故B错误;
C.甲氢氧化钠和碳酸氢钠反应生成碳酸钠和水,容器内压强不变,所以气球不变;乙中澄清石灰水和碳酸氢钠之间反应没有气体生成,使容器内压强不变,所以气球不变,故C错误;
D.甲中盐酸和碳酸氢钠之间反应生成二氧化碳,容器内压强增大,所以气球变大;乙中氢氧化钠和二氧化碳之间反应,使容器内压强小于大气压,所以气球变大,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、反应原理及实验装置的作用为解答的关键,侧重分析与应用能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
12.下列说法正确的是( )
| A. | 酒精、硫酸钡和水分别属于电解质、强电解质和弱电解质 | |
| B. | Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 | |
| C. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| D. | 天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源 |
13.向20mL 0.1mol/L NH4HSO4溶液中滴入0.1mol/L NaOH溶液,下列说法正确的是( )
| A. | 整个反应过程中:c(H+)+c(Na+)+c(NH4+)=c(OH-)+c(SO42-) | |
| B. | 当滴入30mL NaOH溶液时(pH>7):c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| C. | 当滴入20mL NaOH溶液时:2c(SO42-)═c(NH3•H2O)+c(NH4+) | |
| D. | 当溶液呈中性时:c(NH4+)>c(SO42-)>c(Na+)>c(H+)=c(OH-) |
10.下列有关物质的性质和该性质的应用均正确的是( )
| A. | NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体 | |
| B. | NaHCO3能与碱反应,食品工业上用作焙制糕点的膨松剂 | |
| C. | Mg(OH)2分解吸热且生成高熔点固体,可用作阻燃剂 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
11.某原电池的总反应为:Cu+2Fe3+═Cu2++2Fe2+( )
| A | B | C | D | |
| 电极材料 | Cu、Zn | Cu、Ag | Fe、Zn | Cu、C |
| 插入溶液 | FeCl3 | Fe(NO3) 2 | CuSO4 | Fe2(SO4)3 |
| A. | A | B. | B | C. | C | D. | D |
12.下列实验中,直接采用沾有水滴的仪器,对实验结果没有影响的是( )
| A. | 氨的喷泉实验:圆底烧瓶 | B. | 实验室制氧气:试管 | ||
| C. | 中和滴定:锥形瓶 | D. | 中和滴定:滴定管 |
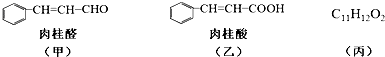
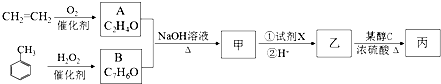
 .
. $→_{△}^{氢氧化钠溶液}$
$→_{△}^{氢氧化钠溶液}$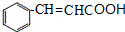 +H2O.
+H2O.
 ;
;