题目内容
6.NA为阿伏加罗常数的值,下列说法正确的是( )| A. | 利用大阳能制氢时,若光解0.02molH2O可生成H2的质量为0.02g | |
| B. | 用生氢剂CaH2与水反应制氢时,生成1mol H2时转移电子致目为2NA | |
| C. | 常温常压下,4.0g氢氧化钠溶于1L水所得溶液c(NaOH)=0.10mol/L | |
| D. | 标准状况下,22.4LCH3Cl中含有的共用电子对数目为4NA |
分析 A、光解0.02mol水可以生成0.02mol氢气,根据质量m=nM来计算其质量;
B、用生氢剂CaH2与水反应制氢时,发生的是归中反应;
C、氢氧化钠溶于1L水后,溶液体积大于1L;
D、求出一氯甲烷的物质的量,然后根据一氯甲烷中含4对共用电子对来分析.
解答 解:A、光解0.02mol水可以生成0.02mol氢气,质量m=nM=0.2mol×2g/mol=0.4g,故A错误;
B、用生氢剂CaH2与水反应制氢时,发生的是归中反应,故生成1mol氢气转移1mol电子即NA个,故B错误;
C、氢氧化钠溶于1L水后,溶液体积大于1L,故溶液中氢氧化钠的物质的量浓度小于0.1mol/L,故C错误;
D、标况下22.4L一氯甲烷的物质的量为1mol,而一氯甲烷中含4对共用电子对,故1mol一氯甲烷中含4NA对共用电子对,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
18.常温下,下列反应产生氢气最多的是( )
| A. | 1.12 g铁与足量浓硫酸反应 | |
| B. | 0.12g镁与足量盐酸反应 | |
| C. | 0.02mol钠与足量水反应 | |
| D. | 0.01mol铝与足量氢氧化钠溶液反应 |
17.一定温度下,某容器中加入足量的碳酸钙,发生反应CaCO3(s)?CaO(s)+CO2(g)达到平衡.下列说法正确的是( )
| A. | 将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度为原来的2倍 | |
| B. | CaCO3(s)加热分解成CaO(s)和CO2(g),△S<0 | |
| C. | 将体积增大为原来的2倍,再次达到平衡时,平衡向正方向移动 | |
| D. | 保持容器体积不变,充入He,平衡向逆反应方向进行 |
14.现有碳酸钾和碳酸氢钾的混合物样品,为测记其组成,分别称取三份不同质量的该混合物样品,配成溶液,然后用相同浓度的硫酸进行滴定,已知:CO32-”与H+反应生成CO2,分两步:CO32-+H+=HCO3-+H+=CO2↑+H2O
下列说法正确的是( )
| 实验编号 | 1 | 1 | 3 |
| 混合物的体积/g | 3.76 | 4.70 | 8.46 |
| 硫酸浓液的体积/mL | 50.00 | 50.00 | 50.00 |
| 生成一氧化碳的物质的量/mol | 0.03 | 0,0375 | 0.03 |
| A. | 样品中碳酸钾和碳酸氢钾的物成的量之比为1:2 | |
| B. | 样品中碳酸钾和碳酸氢钾的物质的量之比为2:3 | |
| C. | 所用硫酸的物质的量浓度为l.5mol•L-1 | |
| D. | 所用嫌酸的物质的量浓度为0.75mol•L-1 |
1.将一铁、铜混合物粉末平均分成三等份,分别加入到同浓度、不同体积的稀硝酸中,充分反应后,收集到NO气体的体积及剩余固体的质量如表 (设反应前后溶液的体积不变,气体体积已换算为标准状况时的体积):
下列说法正确的是( )
| 实验序号号 | 稀硝酸的体积/mL | 剩余固体的质量/g | NO的体积/L |
| 1 | 100 | 17.2 | 2.24 |
| 2 | 200 | 8.00 | 4.48 |
| 3 | 400 | 0 | V |
| A. | 表中 V=7.84 L | |
| B. | 原混合物粉末的质量为25.6 g | |
| C. | 原混合物粉未中铁和铜的物质的量之比为2:3 | |
| D. | 实验3所得溶液中硝酸的物质的量浓度为0.875 mol•L-1 |
11.下列物质的水溶液因水解而呈酸性的是( )
| A. | NaHSO3 | B. | AgNO3 | C. | H2CO3 | D. | NaCl |
18.下列各组中,两种气体的原子数一定相等的是( )
| A. | 温度相同、体积相同的O2和O3 | B. | 质量相等、密度不等的C2H6和NO | ||
| C. | 质量相等、密度不等的CO和N2 | D. | 体积相等、密度相等的CO2和N2O |
16.已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构.关于ABCD四种元素的叙述正确的是( )
| A. | 原子序数a>b>c>d | |
| B. | 最高价氧化物对应水化物的碱性B>A | |
| C. | 单质还原性A>B>C>D | |
| D. | 离子半径D(n+1)->Cn->An+>B(n+1)+ |

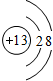 ,MgO的电子式
,MgO的电子式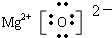 .
.