题目内容
8.M是石油裂解气的重要成分,由M制备环酯P的合成路线(部分反应条件略去)如图所示: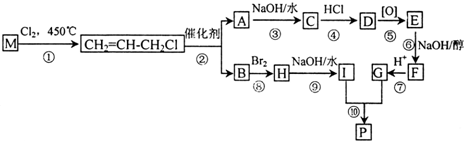
已知:在特殊催化剂的作用下能够发生碳碳双键两边基团互换位置的反应.如:
2CH2=CHR$\stackrel{催化剂}{→}$CH2=CH2+RCH=CHR
回答下列问题:
(1)M的名称是丙烯,A含有的官能团名称是碳碳双键、氯原子.
(2)①的反应类型是取代反应,⑥的反应类型是消去反应.
(3)C的结构简式为HOCH2CH=CHCH2OH.由C→G的过程中步骤④、⑥的目的是保护分子中碳碳双键不被氧化,.
(4)G中最多有12个原子共平面,其顺式结构式为
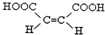 .
.(5)符合下列条件D的同分异构体有10种.
①氯原子连在碳链的一端 ②羟基连在不同的碳原子上,其中核磁共振氢谱为4组峰且峰面积比为4:2:2:1的为ClCH2CH(CH2OH)2(写结构简式).
(6)由I和G在一定条件下制取环酯P的化学方程式为
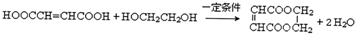 .
.
分析 M是石油裂解气的重要成分,与氯气发生取代反应生成CH2=CHCH2Cl,则M为CH2=CHCH3.由反应信息可知,CH2=CHCH2Cl在催化剂条件下生成CH2=CH2、ClCH2CH=CHCH2Cl,A在氢氧化钠水溶液、加热条件下发生反应,故A为ClCH2CH=CHCH2Cl,B为CH2=CH2.B与溴发生加成反应生成H,H为BrCH2CH2Br,H在氢氧化钠水溶液、加热条件下发生取代反应生成I,I为HOCH2-CH2OH.A在氢氧化钠水溶液、加热条件下发生反应生成C,C为HOCH2CH=CHCH2OH,C生成D是C与HCl的加成反应,故D为HOCH2CH2CHClCH2OH,D发生氧化反应生成E,E发生消去反应生成F,F酸化得到G,而G与I发生酯化反应生成环酯P,则E为
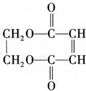 .
.
解答 解:M是石油裂解气的重要成分,与氯气发生取代反应生成CH2=CHCH2Cl,则M为CH2=CHCH3.由反应信息可知,CH2=CHCH2Cl在催化剂条件下生成CH2=CH2、ClCH2CH=CHCH2Cl,A在氢氧化钠水溶液、加热条件下发生反应,故A为ClCH2CH=CHCH2Cl,B为CH2=CH2.B与溴发生加成反应生成H,H为BrCH2CH2Br,H在氢氧化钠水溶液、加热条件下发生取代反应生成I,I为HOCH2-CH2OH.A在氢氧化钠水溶液、加热条件下发生反应生成C,C为HOCH2CH=CHCH2OH,C生成D是C与HCl的加成反应,故D为HOCH2CH2CHClCH2OH,D发生氧化反应生成E,E发生消去反应生成F,F酸化得到G,而G与I发生酯化反应生成环酯P,则E为
 .
.
(1)M为CH2=CHCH3,M的名称是丙烯,A为ClCH2CH=CHCH2Cl,A含有的官能团名称是碳碳双键、氯原子,
故答案为:丙烯;碳碳双键、氯原子;
(2)①的反应类型是取代反应,⑥的反应类型是消去反应,
故答案为:取代反应;消去反应;
(3)C的结构简式为HOCH2CH=CHCH2OH,由C→G的过程中步骤④、⑥的目的是:保护分子中碳碳双键不被氧化,
故答案为:HOCH2CH=CHCH2OH;保护分子中碳碳双键不被氧化;
(4)G为HOOC-CH=CH-COOH,碳碳双键、碳氧双键均为平面结构,旋转碳碳双键,平面可以共面,旋转C-O单键可以使羟基中H原子处于平面内,分子中的12个原子都可以共面,其顺式结构式为 ,
,
故答案为:12; ;
;
(5)D为HOCH2CH2CHClCH2OH,D的同分异构体中Cl原子位于端头碳原子上,且羟基连在不同的碳原子上的有ClCH2CH(OH)CH2CH2OH、ClCH2CH2CH(OH)CH2OH、ClCH(OH)CH2CH2CH2OH、ClCH2CH(OH)CH(OH)CH3、ClCH(OH)CH2CH(OH)CH3、ClCH(OH)CH(OH)CH2CH3、ClCH(OH)C(CH3)2OH、ClCH(OH)CH(CH3)CH2OH、ClCH2C(OH)(CH3)CH2OH、ClCH2CH(CH2OH)2,共10种,其中核磁共振氢谱为4组峰,且峰面积比为4:2:2:1的为 ClCH2CH(CH2OH)2,
故答案为:10;ClCH2CH(CH2OH)2;
(6)由I和G在一定条件下制取环酯P的化学方程式为: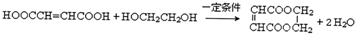 ,
,
故答案为: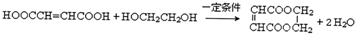 .
.
点评 本题考查有机物推断,侧重考查学生分析推断能力及信息获取利用能力,根据某些物质结构简式、反应条件、题给信息结合有机物官能团及其性质进行推断,难点是(5)题同分异构体种类判断,注意限制性条件,题目难度中等.

 金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:
金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:(1)Ti的基态原子价电子排布式为3d24s2.
(2)纳米TiO2常用作下述反应的催化剂.
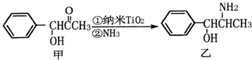
化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C.
(3)含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2•H2O,其配离子中含有的化学键类型是共价键、配位键,1mol该配合物中含有的σ键数目是18NA.
(4)通过X-射线探知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
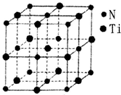
(5)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有12个:Ti原子的配位数为6;此配位原子构成的空间构型为正八面体;该晶胞中N、Ti原子之间的最近距离为a nm.则该氮化钛晶体的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-7})^{3}}$g•cm-3、NA为阿伏加德罗常数的值,只列计算式).
| A. | 241 | B. | 146 | C. | 95 | D. | 336 |
| A. | X、Y、Z的热稳定性逐渐增强 | |
| B. | A、B、C、D只能形成5种单质 | |
| C. | A、B的氧化物的水化物的酸性逐渐增强 | |
| D. | 由B、C、D三种元素组成的化合物中只能形成共价键 |
| 编号 | 现象或操作 | 解释或结论 |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去 | SO2具有漂白性 |
| B | 在0.1mol•L-1的CH3COONa溶液中,加2滴酚酞显浅红色,微热,溶液颜色加深 | 盐类水解反应是吸热反应 |
| C | 向少量火柴头的浸泡溶液中滴加AgNO3、HNO3和NaNO2混合溶液后,产生白色沉淀 | 火柴头里含有氯元素 |
| D | 蒸馏时,温度计的球泡应靠近蒸馏烧瓶支管口处 | 此位置指示的是馏出物的沸点 |
| A. | A | B. | B | C. | C | D. | D |
| A. | MgSO4溶液与Ba(OH)2溶液混合:Ba2++SO42-=BaSO4↓ | |
| B. | 0.3 mol FeBr2与0.4 mol Cl2在溶液中反应:8Cl2+6Fe2++10Br-=6Fe3++16Cl-+5Br2 | |
| C. | Cu与稀HNO3反应:Cu+4H++2NO3-=Cu2++2NO↑+2H2O | |
| D. | AgCl固体溶于足量氨水:Ag++2NH3•H2O=[Ag(NH3)2]++2H2O |

 Li2CO3+Li2SiO3;该反应为放(填“吸”或者“放”)热反应,原因是升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应.
Li2CO3+Li2SiO3;该反应为放(填“吸”或者“放”)热反应,原因是升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应.