题目内容
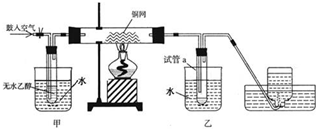
 实验室制取乙烯的装置如图所示,请回答:
实验室制取乙烯的装置如图所示,请回答:(1)反应中浓硫酸起
(2)烧瓶内放碎瓷片的作用是
(3)制取乙烯的化学方程式是:
(4)可能生成的主要有机副产物是
考点:乙烯的实验室制法
专题:
分析:(1)实验室用乙醇加热制取乙烯,该反应中浓硫酸作催化剂和脱水剂;
(2)烧瓶内放碎瓷片目的是防止暴沸而引起安全事故;
(3)在浓硫酸作催化剂、170℃条件下,乙醇发生消去反应生成乙烯和水;
(4)在浓硫酸作催化剂、140℃条件下,乙醇发生分子间脱水生成乙醚.
(2)烧瓶内放碎瓷片目的是防止暴沸而引起安全事故;
(3)在浓硫酸作催化剂、170℃条件下,乙醇发生消去反应生成乙烯和水;
(4)在浓硫酸作催化剂、140℃条件下,乙醇发生分子间脱水生成乙醚.
解答:
解:(1)实验室用乙醇加热制取乙烯,该反应中浓硫酸将乙醇中的H、O元素以2:1水的形式脱去而体现脱水性,同时浓硫酸能加快反应速率缩短反应时间,从而体现催化能力,所以浓硫酸作催化剂和脱水剂,
故答案为:催化;脱水;
(2)烧瓶内放碎瓷片目的是防止液体剧烈沸腾而引起安全事故,故答案为:防暴沸;
(3)在浓硫酸作催化剂、170℃条件下,乙醇发生消去反应生成乙烯和水,反应方程式为CH3CH2OH
CH2=CH2↑+H2O,
故答案为:CH3CH2OH
CH2=CH2↑+H2O;
(4)在浓硫酸作催化剂、140℃条件下,乙醇发生分子间脱水生成乙醚,所以其副产物主要是乙醚,发生的反应方程式为2CH3CH2OH
CH3CH2OCH2CH3+H2O,
故答案为:乙醚;2CH3CH2OH
CH3CH2OCH2CH3+H2O.
故答案为:催化;脱水;
(2)烧瓶内放碎瓷片目的是防止液体剧烈沸腾而引起安全事故,故答案为:防暴沸;
(3)在浓硫酸作催化剂、170℃条件下,乙醇发生消去反应生成乙烯和水,反应方程式为CH3CH2OH
| 浓H2SO4 |
| 170℃ |
故答案为:CH3CH2OH
| 浓H2SO4 |
| 170℃ |
(4)在浓硫酸作催化剂、140℃条件下,乙醇发生分子间脱水生成乙醚,所以其副产物主要是乙醚,发生的反应方程式为2CH3CH2OH
| 浓H2SO4 |
| 140℃ |
故答案为:乙醚;2CH3CH2OH
| 浓H2SO4 |
| 140℃ |
点评:本题考查乙烯的实验室制法,侧重考查实验操作、物质性质,注意乙醇生成乙烯、乙醚时断键方式的区别,生成乙烯属于消去反应、生成乙醚属于取代反应,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列解释事实的离子方程式正确的是( )
| A、铁和稀硝酸反应制得浅绿色溶液:Fe+4H++NO3-═Fe3++NO↑+2H2O |
| B、实验室盛碱液的瓶子不用玻璃塞:SiO2+2OH-═SiO32-+H2O |
| C、碳酸氢镁和足量的氢氧化钙溶液反应:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| D、向Ca(ClO)2溶液中通入过量CO2:2ClO-+H2O+CO2═2HClO+CO32- |
下列表示物质的图或式正确的是( )
| A、氮气的电子式N┇┇N |
B、Mg2+的结构示意图 |
C、NH3的结构式  |
D、CO2的电子式  |
下列各组物质互为同位素的是( )
| A、金刚石和石墨 |
| B、16O2和16O3 |
| C、H2O和D2O |
| D、12C和14C |
已知C3N4晶体很可能具有比金刚石更大的硬度,且原子间以单键结合.下列有关C3N4晶体的说法中正确的是( )
| A、C3N4晶体是分子晶体 |
| B、C3N4晶体中C-N键的键长比金刚石中的C-C键的键长短 |
| C、C3N4晶体中C、N原子个数之比为4:3 |
| D、C3N4晶体中微粒间通过离子键结合 |
A、B两种元素以共价键相结合成AB2型化合物,则A、B两种元素在周期表中的族不可能是下列的( )
| A、ⅣA、ⅥA |
| B、ⅥA、ⅦA |
| C、VA、ⅥA |
| D、ⅡA、ⅦA |
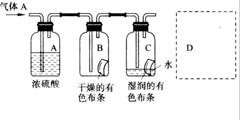 某学生用如图所示的方法研究物质的性质,其中气体A的主要成分,杂质是空气和水蒸气,回答下列问题:
某学生用如图所示的方法研究物质的性质,其中气体A的主要成分,杂质是空气和水蒸气,回答下列问题: 现有 aA、bB、CC、dD、eE、gG六种短周期非金属元素,a+b=c,a+c=d,a+d=e,d+e=g,C、E、G的单质圴有在中学常见的两种或多种同素异形体.请回答下列问题:
现有 aA、bB、CC、dD、eE、gG六种短周期非金属元素,a+b=c,a+c=d,a+d=e,d+e=g,C、E、G的单质圴有在中学常见的两种或多种同素异形体.请回答下列问题: