题目内容
18.钠、铝和铁是三种重要的金属.请回答:Ⅰ、(1)钠原子的结构示意图是
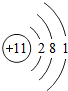 ;铝原子的结构示意图是
;铝原子的结构示意图是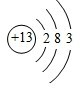 .
.(2)将一小块金属钠长期露置于空气中发生一系列变化,最终产物是Na2CO3.
(3)取一小块金属钠放在滴有酚酞的水中,实验现象正确的是(填选项)①③④⑤.
①钠浮在水面迅速反应 ②钠沉在水底迅速反应 ③钠熔成小球并快速游动 ④反应中可以听到嘶嘶的响声 ⑤反应后的溶液变为红色
Ⅱ(1)写出这三种金属中能与氢氧化钠溶液反应的离子方程式2Al+2H2O+2OH-═2AlO2-+3H2↑
(2)铁、铝是常用的金属材料,在空气中铝比铁更耐腐蚀.对此合理的解释是在常温下,金属铝表面可以形成一层致密的氧化膜.
分析 Ⅰ、(1)钠原子核外有11电子;铝原子核外有13电子;
(2)Na的性质活泼,易与空气中氧气反应生成Na2O,Na2O易与水反应生成NaOH,NaOH吸收空气中的水和CO2生成Na2CO3•xH2O,Na2CO3•xH2O风化脱水生成Na2CO3;
(3)Na的密度小于水,钠的熔点较低,钠和水反应生成NaOH和氢气同时放出大量热,钠受力不均导致四处游动;
Ⅱ(1)三种金属中只有铝能与氢氧化钠溶液反应生成偏铝酸钠和氢气;
(2)在常温下,金属铝表面可以形成一层致密的氧化膜,能阻碍金属继续与空气反应.
解答 解:Ⅰ、(1)钠原子核外有11电子,则钠原子的结构示意图是 ;铝原子核外有13电子,则铝原子的结构示意图是
;铝原子核外有13电子,则铝原子的结构示意图是 ,故答案为:
,故答案为: ;
; ;
;
(2)Na的性质活泼,易与空气中氧气反应生成Na2O,Na2O易与水反应生成NaOH,NaOH吸收空气中的水和CO2生成Na2CO3•xH2O,Na2CO3•xH2O风化脱水生成Na2CO3,所以将一小块金属钠长期露置于空气中发生一系列变化,最终产物是Na2CO3,故答案为:Na2CO3;
(3)Na的密度小于水,所以钠会浮在水面上,钠的熔点较低,钠和水反应生成NaOH和氢气同时放出大量热使钠熔融发出嘶嘶的响声,钠受力不均导致四处游动,生成NaOH导致溶液呈碱性,则溶液变红色,所以实验现象正确的是①③④⑤;故答案为:①③④⑤;
Ⅱ、(1)三种金属中只有铝能与氢氧化钠溶液反应生成偏铝酸钠和氢气,离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,故答案为:2Al+2H2O+2OH-═2AlO2-+3H2↑;
(2)在常温下,金属铝表面可以形成一层致密的氧化膜,能阻碍金属继续与空气反应;
故答案为:在常温下,金属铝表面可以形成一层致密的氧化膜.
点评 本题考查了金属的反应,明确金属的性质是解本题关键,根据铝、钠、铁的性质分析解答,注意铁和水蒸气反应的生成物.

| A. | 单位时间内生成n mol X2,同时生成n mol XY | |
| B. | 单位时间内生成n mol X2,同时生成n mol Y2 | |
| C. | 单位时间内生成2n mol XY,同时生成n mol Y2 | |
| D. | 容器内总压强不随时间变化 |
| A. | H2O(g)→H2O(1)+44.0kJ | B. | 2HI(g)→H2(g)+I2(g)-9.4kJ | ||
| C. | 浓硫酸溶于水 | D. | 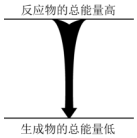 能量变化如图所示的化学反应 |
| A. | 摩尔质量:mol/g | B. | 物质量:mol | ||
| C. | 溶解度:g/100g | D. | 气体摩尔体积:L/mol |

 $→_{△}^{浓硫酸}$R-CH=CH2+H2O,叫做消去反应
$→_{△}^{浓硫酸}$R-CH=CH2+H2O,叫做消去反应


