题目内容
18.在CO2中,Mg燃烧生成MgO和C.下列说法正确的是( )| A. | 该反应属于置换反应 | |
| B. | ${\;}_{\;}^{12}$C和${\;}_{\;}^{14}$C是碳元素的两种同素异形体 | |
| C. | 该反应中化学能全部转化为热能 | |
| D. | 在该反应条件下,C的还原性强于Mg的还原性 |
分析 在CO2中,Mg燃烧生成MgO和C,反应方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO,
A.一种单质和一种化合物反应生成另外的单质和化合物为置换反应;
B.质子数相同、中子数不同的同一元素的原子互称同位素,同种元素的不同单质互称同素异形体;
C.该反应中部分化学能转化为热能、部分转化为光能;
D.同一氧化还原反应中,还原剂的还原性大于还原产物的还原性.
解答 解:在CO2中,Mg燃烧生成MgO和C,反应方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO,
A.一种单质和一种化合物反应生成另外的单质和化合物为置换反应,镁置换出C,所以属于置换反应,故A正确;
B.质子数相同、中子数不同的同一元素的原子互称同位素,同种元素的不同单质互称同素异形体,${\;}_{\;}^{12}$C和${\;}_{\;}^{14}$C是质子数相同、中子数不同的同一元素不同原子,互称同位素,故B错误;
C.该反应中部分化学能转化为热能、部分转化为光能,故C错误;
D.同一氧化还原反应中,还原剂的还原性大于还原产物的还原性,该反应中Mg是还原剂、C是还原产物,所以Mg的还原性大于C,故D错误;
故选A.
点评 本题以Mg为载体考查基本概念、基本理论,明确概念内涵是解本题关键,注意同位素、同素异形体区别,注意:镁在氧气、氮气及二氧化碳中都能燃烧,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.元素周期律(表)是认识元素化合物性质的重要理论.
(1)某学习小组研究了金属锂、钠、镁的性质后发现:
ⅰ.锂、镁和水反应均较为微弱,钠和水反应较为剧烈.
ⅱ.锂和镁的氢氧化物均为中等强度的碱.
ⅲ.锂、镁在空气中燃烧均生成氧化物,而钠在空气中燃烧生成过氧化物.
由以上事实,可知锂、钠、镁三种元素的金属性强弱关系是Na>Mg=Li.
(2)锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族.
①碱性:Sr(OH)2< Ba (OH)2(填“>”或“<”).
②用原子结构的观点解释锶的化学性质与钡差异的原因:锶和钡位于同一主族,锶的电子层数比钡少,原子半径小,失电子能力弱,金属性弱.
(3)硒(Se)的部分信息如右图,且知34Se、35Br位于同一周期.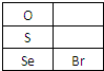
①Se在元素周期表中的位置是第四周期第VIA族.
②H2Se的电子式是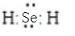 .
.
③Cl、Se、Br的非金属性强弱的顺序是Cl>Br>Se.
能证明上述非金属性强弱关系的事实是氢化物的稳定性(写出一条即可).
④某同学对SeO2(白色的挥发性固体,易溶于水)的各种不同化学性质进行推测,并用SO2水溶液、H2O2溶液、NaOH溶液、稀H2SO4等试剂进行实验,证明了推测是正确的.
完成下表:
(1)某学习小组研究了金属锂、钠、镁的性质后发现:
ⅰ.锂、镁和水反应均较为微弱,钠和水反应较为剧烈.
ⅱ.锂和镁的氢氧化物均为中等强度的碱.
ⅲ.锂、镁在空气中燃烧均生成氧化物,而钠在空气中燃烧生成过氧化物.
由以上事实,可知锂、钠、镁三种元素的金属性强弱关系是Na>Mg=Li.
(2)锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族.
①碱性:Sr(OH)2< Ba (OH)2(填“>”或“<”).
②用原子结构的观点解释锶的化学性质与钡差异的原因:锶和钡位于同一主族,锶的电子层数比钡少,原子半径小,失电子能力弱,金属性弱.
(3)硒(Se)的部分信息如右图,且知34Se、35Br位于同一周期.

①Se在元素周期表中的位置是第四周期第VIA族.
②H2Se的电子式是
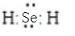 .
.③Cl、Se、Br的非金属性强弱的顺序是Cl>Br>Se.
能证明上述非金属性强弱关系的事实是氢化物的稳定性(写出一条即可).
④某同学对SeO2(白色的挥发性固体,易溶于水)的各种不同化学性质进行推测,并用SO2水溶液、H2O2溶液、NaOH溶液、稀H2SO4等试剂进行实验,证明了推测是正确的.
完成下表:
| 编号 | 性质推测 | 化学方程式 |
| 1 | 氧化性 | SeO2+2SO2+2H2O═Se+2H2SO4 |
| 2 | 还原性 | SeO2+2H2O2=H2SeO4+2H2O |
| 3 | 酸性氧化物 | SeO2+NaOH=Na2SeO3+H2O |
13.下列离子方程式错误的是( )
| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 向Ca(HCO3)2溶液中滴加少量NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | 等物质的量的MgCl2、Ba(OH)2、HCl三种溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| D. | 氢氧化钠溶液中通入氯气:Cl2+2OH-═ClO-+Cl-+H2O |
3.原子序数依次增大的四种短周期元素X、Y、Z、W,其中Y、Z、W同周期,X和W同主族,简单离子半径的大小为X->Y+,其中Z为地壳中含量最高的金属元素,则下列说法正确的是( )
| A. | X和W元素的最高正价相同 | |
| B. | Y、Z均为金属元素,故X、Y、Z三种元素不能形成化合物 | |
| C. | 工业上常利用电解ZW3溶液冶炼金属Z | |
| D. | Y、W的最高价氧化物水化物均能溶解Z单质 |
10.设NA为阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 标准状况下,78g苯中含有碳氢键的数目为6NA | |
| B. | 180g乙酸、葡萄糖的混合物所含碳原子数为6NA | |
| C. | 1L0.1mol•L-1Na2S溶液中阴离子总数大于0.1NA | |
| D. | 在密闭容器中通入3molH2和1molN2,充分反应后得到的NH3分子数为2NA |
7.在进行牙科治疗之前,吸入笑气(N2O)能明显减轻牙科焦虑症.同温同压下,相同质量的下列气体与笑气体积相等的是( )
| A. | N2 | B. | CO | C. | CO2 | D. | NO2 |
8.下列各组物质属于同系物的是( )
| A. | H2和D2 | B. | 苯和甲苯 | C. | 正丁烷和异丁烷 | D. | 葡萄糖和果糖 |
 中学实验室用如图装置制取少量溴苯,在烧瓶a中装的试剂是苯、液溴和铁粉,d中装的是蒸馏水.请回答下列问题.
中学实验室用如图装置制取少量溴苯,在烧瓶a中装的试剂是苯、液溴和铁粉,d中装的是蒸馏水.请回答下列问题.