题目内容
7.五种短周期元素X、Y、Z、W、M,X的质子总数与电子层数相同,Y、Z、W、M在周期表中的位置如图所示,其中W的单质是一种重要的半导体材料.下列说法不正确的是( )| Y | Z | M |
| W |
| A. | 原子半径大小关系为:W>Y>Z>M>X | |
| B. | 最高价氧化物对应的水化物酸性:W<Y<Z | |
| C. | 分子式为X5YZM2的化合物中含有离子键和共价键 | |
| D. | 元素Y、W的单质一定属于同种类型的晶体 |
分析 X、Y、Z、M、W为5种短周期元素,X的质子总数与电子层数相同,则X为H元素;其中W的单质是一种重要的半导体材料,所以w是Si,所以Y是C,Z是N,M是O,由此分析解答.
解答 解:X、Y、Z、M、W为5种短周期元素,X的质子总数与电子层数相同,则X为H元素;其中W的单质是一种重要的半导体材料,所以w是Si,所以Y是C,Z是N,M是O,
A.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Si>N>O>F>H,故A正确;
B.Si、C、N三种元素对应的酸分别是硅酸、碳酸和硝酸以,酸性强弱:硅酸<碳酸<硝酸,故B正确;
C.分子式为X5YZM2的化合物是NH4HC02中含有离子键和共价键,故C正确;
D.晶体硅和金刚石是原子晶体,而碳的单质可能是石墨,所以不一定是同种类型的晶体,故D错误;
故选D.
点评 本题考查结构性质位置关系应用,难度中等,推断元素是解题关键,注意元素周期律在解题中的应用.

练习册系列答案
相关题目
12.萘的结构简式为 ,它与硝酸反应,可生成苯环上的一硝基取代物( )
,它与硝酸反应,可生成苯环上的一硝基取代物( )
 ,它与硝酸反应,可生成苯环上的一硝基取代物( )
,它与硝酸反应,可生成苯环上的一硝基取代物( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
15. (1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol
若有17g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为226.3kJ.
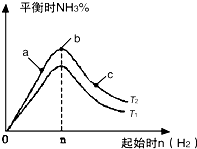
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)?2NH3(g)反应的影响.实验结果如图所示:
(图中T表示温度,n表示物质的量)
①图象中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)═4NO2(g)+O2(g)△H>0下表为反应在T1温度下的部分实验数据
则500s内NO2的平均生成速率为0.00592 mol•L-1•s-1.
 (1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/molN2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol
若有17g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为226.3kJ.
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)?2NH3(g)反应的影响.实验结果如图所示:
(图中T表示温度,n表示物质的量)
①图象中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)═4NO2(g)+O2(g)△H>0下表为反应在T1温度下的部分实验数据
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
2.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2 | |
| B. | 氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ | |
| D. | 钢铁发生电化学腐蚀的负极反应式:Fe-3e-═Fe3+ |
12.检验淀粉、蛋白质、葡萄糖溶液,依次可分别使用的试剂和对应的现象正确的是( )
| A. | 碘水,变蓝色;浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀 | |
| B. | 浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀;碘水,变蓝色 | |
| C. | 新制Cu(OH)2,砖红色沉淀;碘水,变蓝色;浓硝酸,变黄色 | |
| D. | 碘水,变蓝色;新制Cu(OH)2,砖红色沉淀;浓硝酸,变黄色 |
16.只用一种试剂一次性鉴别NH4Cl、Na2SO4、(NH4)2SO4三种物质的试剂是(可加热)( )
| A. | AgNO3 | B. | 稀H2SO4 | C. | 稀HCl | D. | Ba(OH)2溶液 |
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标况下,2.24LHF中所含电子数为0.1NA | |
| B. | 常温常压下,4.4 g乙醛所含σ键数目为0.7NA | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8 NA个电子 | |
| D. | 1 mol Na2O2固体中含离子总数为4NA |
