题目内容
15. (1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/molN2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol
若有17g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为226.3kJ.
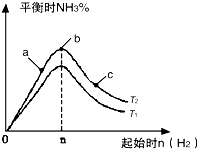
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)?2NH3(g)反应的影响.实验结果如图所示:
(图中T表示温度,n表示物质的量)
①图象中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)═4NO2(g)+O2(g)△H>0下表为反应在T1温度下的部分实验数据
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
分析 (1)根据盖斯定律来求反应的焓变,然后根据反应放出的热量与物质的量成正比来解答;
(2)①根据温度升高化学平衡向着吸热方向进行;
②根据增加氢气的物质的量化学平衡向着正反应方向移动;
(3)500s时,△c(N2O5)=5.00mol/L-3.52mol/L=1.48mol/L,结合v=$\frac{△c}{△t}$计算.
解答 解:(1)①N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol,
②N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ/mol,
③2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol,
由盖斯定律①×2-②×2+③×3得:4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=905kJ/mol;
则17g即1mol氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为$\frac{1}{4}$×905kJ≈226.3kJ,
故答案为:226.3kJ;
(2)①反应为放热反应,温度升高,化学平衡向着吸热方向进行,从T1到T2反应物氨气的量增加,即平衡正向移动,故T1<T2,故答案为:低于;
②b点代表平衡状态,c点又加入了氢气,故平衡向右移动,氮气的转化率增大,故答案为:c;
(3)500s时,△c(N2O5)=5.00mol/L-3.52mol/L=1.48mol/L,则v(N2O5)=$\frac{△c}{△t}$═0.00296mol•L-1•s-1,由速率之比等于化学计量数之比可知,v(NO2)=0.00296mol•L-1•s-1×2=0.00592 mol•L-1•s-1;
故答案为:0.00592 mol•L-1•s-1.
点评 本题主要考查了盖斯定律、外界条件对平衡的影响,反应速率的计算,难度中等,根据课本知识即可完成.

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
| A. | 如图所示的化学反应为放热反应 | |
| B. | 化学反应中有物质变化也有能量变化 | |
| C. | 需要加热的化学反应不一定是吸热反应 | |
| D. | 断裂化学键消耗能量,形成化学键放出能量 |
| Y | Z | M |
| W |
| A. | 原子半径大小关系为:W>Y>Z>M>X | |
| B. | 最高价氧化物对应的水化物酸性:W<Y<Z | |
| C. | 分子式为X5YZM2的化合物中含有离子键和共价键 | |
| D. | 元素Y、W的单质一定属于同种类型的晶体 |
①MnO2+H2O2+2H+=Mn2++O2↑+2H2O
②Mn2++H2O2=MnO2+2H+
下列说法正确的是( )
| A. | H2O2在①中是氧化剂,在②中是还原剂 | |
| B. | 在①中每生成1 mol O2,转移的电子数为1.204×1024 | |
| C. | Mn2+在①中是还原产物,在②中是氧化产物 | |
| D. | 在二氧化锰催化作用下,1 mol H2O2分解生成22.4 L O2 |
| A. | 油脂属于酯类 | B. | 植物油能使溴水褪色 | ||
| C. | 油脂能溶解维生素A | D. | 油脂的水解反应称皂化反应 |