题目内容
16.只用一种试剂一次性鉴别NH4Cl、Na2SO4、(NH4)2SO4三种物质的试剂是(可加热)( )| A. | AgNO3 | B. | 稀H2SO4 | C. | 稀HCl | D. | Ba(OH)2溶液 |
分析 NH4Cl、Na2SO4、(NH4)2SO4三种物质分别与Ba(OH)2溶液反应的现象为:刺激性气体生成、白色沉淀生成、刺激性气体及白色沉淀生成,以此来解答.
解答 解:A.均与硝酸银反应生成白色沉淀,现象相同,不能鉴别,故A不选;
B.均不与稀硫酸反应,现象相同,不能鉴别,故B不选;
C,均与稀盐酸不反应,现象相同,不能鉴别,故C不选;
D.NH4Cl、Na2SO4、(NH4)2SO4三种物质分别与Ba(OH)2溶液反应的现象为刺激性气体生成、白色沉淀生成、刺激性气体及白色沉淀生成,现象不同,可鉴别,故D选;
故选D.
点评 本题考查物质的鉴别,为高频考点,把握物质的性质、性质差异及发生的反应和现象等为解答的关键,侧重分析与实验能力的考查,注意现象相同不能鉴别物质,题目难度不大.

练习册系列答案
相关题目
6.下列说法中错误的是( )


| A. | 如图所示的化学反应为放热反应 | |
| B. | 化学反应中有物质变化也有能量变化 | |
| C. | 需要加热的化学反应不一定是吸热反应 | |
| D. | 断裂化学键消耗能量,形成化学键放出能量 |
7.五种短周期元素X、Y、Z、W、M,X的质子总数与电子层数相同,Y、Z、W、M在周期表中的位置如图所示,其中W的单质是一种重要的半导体材料.下列说法不正确的是( )
| Y | Z | M |
| W |
| A. | 原子半径大小关系为:W>Y>Z>M>X | |
| B. | 最高价氧化物对应的水化物酸性:W<Y<Z | |
| C. | 分子式为X5YZM2的化合物中含有离子键和共价键 | |
| D. | 元素Y、W的单质一定属于同种类型的晶体 |
4.过氧化氢(O为-1价)在二氧化锰催化作用下分解放出氧气的反应机理如下:
①MnO2+H2O2+2H+=Mn2++O2↑+2H2O
②Mn2++H2O2=MnO2+2H+
下列说法正确的是( )
①MnO2+H2O2+2H+=Mn2++O2↑+2H2O
②Mn2++H2O2=MnO2+2H+
下列说法正确的是( )
| A. | H2O2在①中是氧化剂,在②中是还原剂 | |
| B. | 在①中每生成1 mol O2,转移的电子数为1.204×1024 | |
| C. | Mn2+在①中是还原产物,在②中是氧化产物 | |
| D. | 在二氧化锰催化作用下,1 mol H2O2分解生成22.4 L O2 |
11.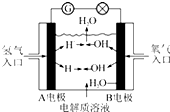 以KOH溶液为电解质溶液的氢氧燃料电池在使用时的电极反应如下:
以KOH溶液为电解质溶液的氢氧燃料电池在使用时的电极反应如下:
2H2+4OH--4e-═4H2O;O2+2H2O+4e-═4OH-.据此作出判断,下列说法正确的是( )
 以KOH溶液为电解质溶液的氢氧燃料电池在使用时的电极反应如下:
以KOH溶液为电解质溶液的氢氧燃料电池在使用时的电极反应如下:2H2+4OH--4e-═4H2O;O2+2H2O+4e-═4OH-.据此作出判断,下列说法正确的是( )
| A. | O2在正极,发生氧化反应 | |
| B. | 供电时的总反应为:2H2+O2═2H2O | |
| C. | 外电路中电流由A电极通过导线流向B电极 | |
| D. | 燃料电池的能量转化率可达100% |
1.下列关于有机化合物的说法正确的是( )
| A. | 甲烷和乙烯都可以与氯气反应 | |
| B. | 酸性高锰酸钾可以氧化苯和甲苯 | |
| C. | 乙烯可以与氢气发生加成反应,苯不能与氢气加成 | |
| D. | 溴乙烷在NaOH的醇溶液中充分反应可得到乙醇 |
8.如图是立方烷的球棍模型,下列有关说法不正确的是( )


| A. | 其一氯代物有二种 | |
| B. | 其二氯代物有三种同分异构体 | |
| C. | 它是一种烃分子 | |
| D. | 它与苯乙烯(CH5-CH═CH2)互为同分异构体 |
5.下列有关油脂的叙述错误的是( )
| A. | 油脂属于酯类 | B. | 植物油能使溴水褪色 | ||
| C. | 油脂能溶解维生素A | D. | 油脂的水解反应称皂化反应 |
6.下列说法中正确的是( )
| A. | 在任何状况下,1 mol CO2和1 mol H2O所含的分子数和原子数都相等 | |
| B. | 只有在标准状况下,1 mol气体所占的体积才是22.4 L | |
| C. | 某物质含有阿伏加德罗常数个微粒,该物质在标准状况下体积为22.4 L | |
| D. | 22.4 L CO所含的分子数为6.02×1023个 |