题目内容
金属元素及其化合物在生产生活中应用日趋广泛,根据相关化学知识,回答下列问题:
(1)金属钠在空气中燃烧的产物常用于呼吸面具中的供氧剂,钠原子的结构示意图为 ,请写出其燃烧产物用作供氧剂的原理 .(用化学方程式表示)
(2)
Mg的中子数为 ,化合物MgO的化学键类型为 .
(3)重铬酸钾(K2Cr2O7)是一种应用广泛的强氧化剂,利用酸性K2Cr2O7的相关性质可以用来检测酒驾.已知将K2CrO4溶于稀硫酸酸化得到重铬酸钾溶液,请写出酸化K2CrO4制备K2Cr2O7溶液的平衡离子方程式: ,这一过程溶液从 色变成 色.
(4)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属以保护轮船外壳,这种金属防护的方法叫做 .
(5)向5.2g Fe3O4、Fe2O3、Cu的混合物中加入0.5mol?L-1的硫酸溶液140mL时,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为 g.
(1)金属钠在空气中燃烧的产物常用于呼吸面具中的供氧剂,钠原子的结构示意图为
(2)
26 12 |
(3)重铬酸钾(K2Cr2O7)是一种应用广泛的强氧化剂,利用酸性K2Cr2O7的相关性质可以用来检测酒驾.已知将K2CrO4溶于稀硫酸酸化得到重铬酸钾溶液,请写出酸化K2CrO4制备K2Cr2O7溶液的平衡离子方程式:
(4)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属以保护轮船外壳,这种金属防护的方法叫做
(5)向5.2g Fe3O4、Fe2O3、Cu的混合物中加入0.5mol?L-1的硫酸溶液140mL时,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
考点:钠的化学性质,氧化还原反应,有关混合物反应的计算
专题:
分析:(1)钠原子的结构示意图为 ;钠在空气中燃烧生成过氧化钠,过氧化钠能和二氧化碳、水反应生成氧气;
;钠在空气中燃烧生成过氧化钠,过氧化钠能和二氧化碳、水反应生成氧气;
(2)中子数=质量数-质子数;根据化合物MgO为离子化合物分析;
(3)K2CrO4溶于稀硫酸酸化得到重铬酸钾溶液,离子方程式为:2CrO42-+2H+?Cr2O72-+H2O;根据K2CrO4为黄色,重铬酸钾溶液为橙色分析;
(4)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属以保护轮船外壳,这种金属防护的方法叫做牺牲阳极的阴极保护法;
(5)Fe3O4、Fe2O3、Cu的混合物中加入硫酸溶液中,固体恰好完全溶解,所得溶液中不含Fe3+,溶液中溶质为CuSO4、FeSO4,硫酸中H元素与混合物中O元素结合守恒水,由水的分子式H2O可知,故n(O)=n(H2SO4),若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为混合物中氧元素的质量.
 ;钠在空气中燃烧生成过氧化钠,过氧化钠能和二氧化碳、水反应生成氧气;
;钠在空气中燃烧生成过氧化钠,过氧化钠能和二氧化碳、水反应生成氧气;(2)中子数=质量数-质子数;根据化合物MgO为离子化合物分析;
(3)K2CrO4溶于稀硫酸酸化得到重铬酸钾溶液,离子方程式为:2CrO42-+2H+?Cr2O72-+H2O;根据K2CrO4为黄色,重铬酸钾溶液为橙色分析;
(4)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属以保护轮船外壳,这种金属防护的方法叫做牺牲阳极的阴极保护法;
(5)Fe3O4、Fe2O3、Cu的混合物中加入硫酸溶液中,固体恰好完全溶解,所得溶液中不含Fe3+,溶液中溶质为CuSO4、FeSO4,硫酸中H元素与混合物中O元素结合守恒水,由水的分子式H2O可知,故n(O)=n(H2SO4),若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为混合物中氧元素的质量.
解答:
解:(1)钠原子的结构示意图为 ;钠在空气中燃烧生成过氧化钠,过氧化钠能和二氧化碳、水反应生成氧气,所以常用于呼吸面具中的供氧剂,发生的反应为:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,
;钠在空气中燃烧生成过氧化钠,过氧化钠能和二氧化碳、水反应生成氧气,所以常用于呼吸面具中的供氧剂,发生的反应为:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,
故答案为: ;2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑;
;2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑;
(2)中子数=质量数-质子数,所以)
Mg的中子数为26-12=14;因为化合物MgO为离子化合物,所以MgO的化学键类型为离子键,
故答案为:14;离子键;
(3)K2CrO4溶于稀硫酸酸化得到重铬酸钾溶液,离子方程式为:2CrO42-+2H+?Cr2O72-+H2O;因为K2CrO4为黄色,重铬酸钾溶液为橙色,所以颜色从黄色变成橙色;故答案为:2CrO42-+2H+?Cr2O72-+H2O;黄;橙;
(4)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属以保护轮船外壳,这种金属防护的方法叫做牺牲阳极的阴极保护法,
故答案为:牺牲阳极的阴极保护法;
(5)Fe3O4、Fe2O3、Cu的混合物中加入硫酸溶液中,固体恰好完全溶解,所得溶液中不含Fe3+,溶液中溶质为CuSO4、FeSO4,硫酸中H元素与混合物中O元素结合守恒水,由水的分子式H2O可知,故n(O)=n(H2SO4)=0.14L×0.5mol/L=0.07mol,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为氧化物中氧元素的质量,所以固体减少的质量为0.07mol×16g/mol=1.12g,
故答案为:1.12
 ;钠在空气中燃烧生成过氧化钠,过氧化钠能和二氧化碳、水反应生成氧气,所以常用于呼吸面具中的供氧剂,发生的反应为:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,
;钠在空气中燃烧生成过氧化钠,过氧化钠能和二氧化碳、水反应生成氧气,所以常用于呼吸面具中的供氧剂,发生的反应为:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,故答案为:
 ;2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑;
;2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑;(2)中子数=质量数-质子数,所以)
26 12 |
故答案为:14;离子键;
(3)K2CrO4溶于稀硫酸酸化得到重铬酸钾溶液,离子方程式为:2CrO42-+2H+?Cr2O72-+H2O;因为K2CrO4为黄色,重铬酸钾溶液为橙色,所以颜色从黄色变成橙色;故答案为:2CrO42-+2H+?Cr2O72-+H2O;黄;橙;
(4)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属以保护轮船外壳,这种金属防护的方法叫做牺牲阳极的阴极保护法,
故答案为:牺牲阳极的阴极保护法;
(5)Fe3O4、Fe2O3、Cu的混合物中加入硫酸溶液中,固体恰好完全溶解,所得溶液中不含Fe3+,溶液中溶质为CuSO4、FeSO4,硫酸中H元素与混合物中O元素结合守恒水,由水的分子式H2O可知,故n(O)=n(H2SO4)=0.14L×0.5mol/L=0.07mol,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为氧化物中氧元素的质量,所以固体减少的质量为0.07mol×16g/mol=1.12g,
故答案为:1.12
点评:本题考查物质的基本性质以及混合物的有关计算,难度中等,难点为(5)要注意判断氧化物中氧原子的物质的量是解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列烷烃的沸点是:甲烷:-162℃;乙烷:-89℃;丁烷:-1℃;戊烷:36℃.根据以上数字推断丙烷的沸点可能是( )
| A、约-40℃ |
| B、约-182℃ |
| C、约-108℃ |
| D、约56℃ |
下列说法中正确的是( )
| A、摩尔是用于计量微观粒子集体的物理量 |
| B、CO2的摩尔质量为44g |
| C、0.5mol水中约含6.02×1023个H |
| D、标准状况下1 mol任何物质体积均为22.4L |
下列与实验相关的叙述正确的是( )
| A、金属钠着火时,可用泡沫灭火器灭火 |
| B、蒸发结晶时应将溶液蒸干 |
| C、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| D、在氢氧化钠溶液中滴入氯化铁饱和溶液可以制得氢氧化铁胶体 |
A、B、C、D四种金属,将AB用导线连接后,浸在稀硫酸中,在A上有氢气放出,而B溶解;当活泼金属浸在含有A和C两种金属离子可溶性盐溶液里时,在活泼金属上先析出C,把D放入B的硝酸盐溶液中,则D表面有B析出.这四种金属的活动性由强到弱的顺序是( )
| A、A>B>C>D |
| B、D>B>A>C |
| C、D>C>B>A |
| D、D>B>C>A |
下列有关电化学中的化学用语,说法正确的是( )
| A、用惰性电极电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| C、粗铜精炼时,与电源正极相连的是纯铜,正极反应式为:Cu2++2e-═Cu |
| D、钢铁发生电化学腐蚀的正极反应式:Fe═Fe2++2e- |
两名日本科学家与一名美国科学家利用钯作催化剂,将有机物进行“裁剪”、“缝合”,创造出具有特殊功能的新物质而获2010年诺贝尔化学奖.下列说法正确的是( )
| A、有机物中一定含有碳和氢两种元素 |
| B、一定条件下,催化剂能提高反应物的转化率 |
| C、将有机物进行“缝合”可以不遵循原子守恒定律 |
| D、将有机物进行“裁剪”需要破坏旧的化学键 |
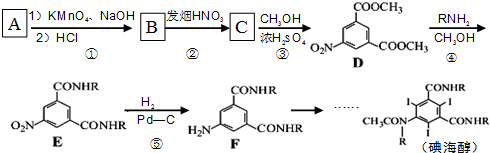
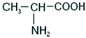 属于α-氨基酸);
属于α-氨基酸);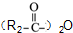 →
→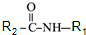 +R2COOH
+R2COOH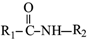 +NaOH→R1COONa+R2NH2
+NaOH→R1COONa+R2NH2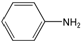 呈弱碱性,易被氧化
呈弱碱性,易被氧化 和(CH3CO)2O为原料制备染料中间体
和(CH3CO)2O为原料制备染料中间体 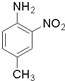 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).