题目内容
现有以下四种物质:A.Si B.FeCl3C.NaHCO3 D.Na2SiO3 请根据题意选择恰当的选项用字母代号填空.
(1)可与KSCN溶液反应,溶液变红的是 ;
(2)常用于焙制糕点,也可用作抗酸药的是 ;
(3)可用于制备硅胶和木材防火剂的是 ;
(4)可用于制造计算机芯片的是 .
(1)可与KSCN溶液反应,溶液变红的是
(2)常用于焙制糕点,也可用作抗酸药的是
(3)可用于制备硅胶和木材防火剂的是
(4)可用于制造计算机芯片的是
考点:硅和二氧化硅,钠的重要化合物,二价Fe离子和三价Fe离子的检验
专题:碳族元素,几种重要的金属及其化合物
分析:(1)三价铁离子与硫氰根离子发生络合反应;
(2)碳酸氢钠不稳定受热易分解,且能够与氯化氢反应;
(3)硅酸钠与酸反应生成硅酸,硅酸钠的水溶液浸泡的木材不易燃烧;
(4)硅导电性介于导体与半导体之间.
(2)碳酸氢钠不稳定受热易分解,且能够与氯化氢反应;
(3)硅酸钠与酸反应生成硅酸,硅酸钠的水溶液浸泡的木材不易燃烧;
(4)硅导电性介于导体与半导体之间.
解答:
解:(1)三价铁离子与硫氰根离子发生络合反应,生成红色络合物,故选B;
(2)碳酸氢钠不稳定受热易分解生成二氧化碳,常用于焙制糕点;能够与盐酸反应消耗氢离子,也可用作抗酸药,故选:C;
(3)硅酸钠与酸反应生成硅酸,可用于制备硅胶;硅酸钠的水溶液浸泡的木材不易燃烧,可以做木材防火剂,故选:D;
(4)硅是良好的半导体材料,可用于制造计算机芯片,故选:A.
(2)碳酸氢钠不稳定受热易分解生成二氧化碳,常用于焙制糕点;能够与盐酸反应消耗氢离子,也可用作抗酸药,故选:C;
(3)硅酸钠与酸反应生成硅酸,可用于制备硅胶;硅酸钠的水溶液浸泡的木材不易燃烧,可以做木材防火剂,故选:D;
(4)硅是良好的半导体材料,可用于制造计算机芯片,故选:A.
点评:本题考查了硅及硅的化合物的用途,性质决定用途,明确性质是解题关键,题目难度不大,注意对基础知识的积累.

练习册系列答案
相关题目
下列方程式中,正确的是( )
| A、氨水中一水合氨的电离方程式:NH3?H2O═NH4-+OH- | |||
| B、氢氧化钡溶液跟稀硫酸反应的离子方程式:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |||
C、苯和硝酸反应的化学方程式: +HNO3 +HNO3
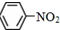 +H2O +H2O | |||
| D、25℃、101 kPa时,1 g甲醇完全燃烧生成CO2和液态水放出22.68 kJ的热量,所以反应物的能量低于生成物的总能量 |
用水稀释0.1mol?L-1氨水时,溶液中随着水量的增加而减小的是 ( )
| A、c(OH-)/c(NH3?H2O) |
| B、c(NH3?H2O)/c(OH-) |
| C、c(H+)和c(OH-)的乘积 |
| D、c(H+) |
下列溶液中各微粒的浓度关系或说法正确的是( )
| A、0.1 mol?L-1 pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
| B、等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、 ④NH3?H2O;c(NH4+) 由大到小的顺序是:①>②>③>④ |
| C、a mol?L-1HCN溶液与b mol?L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b |
| D、0.1mol?L-1的醋酸的pH=a,0.01mol?L-1的醋酸的pH=b,则a+1=b |
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰.在纸内的离子“流过”水和氧化锌组成的电解液.电池总反应为:Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A、该电池的正极为锌 |
| B、该电池反应中二氧化锰起催化剂作用 |
| C、电池负极反应式为:Zn+2OH--2e-═ZnO+H2O |
| D、当 0.l mol Zn 完全溶解时,流经电解液的电子个数为1.204×l023 |