题目内容
 分解水制氢气的工业制法之一是硫--碘循环,主要涉及下列反应:
分解水制氢气的工业制法之一是硫--碘循环,主要涉及下列反应:Ⅰ.SO2+2H2O+I2→H2SO4+2HI;
Ⅱ.2HI?H2+I2;
Ⅲ.2H2SO4→2SO2+O2+2H2O.
(1)分析上述反应,下列判断正确的是
a.反应III易在常温下进行
b.反应I中SO2还原性比HI强
c.循环过程中需补充H2O
d.循环过程中产生1molO2的同时产生1molH2
(2)一定温度下,向2L密闭容器中加入1mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示.0-2min内的平均反应速率v(HI)=
a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
(3)SO2在一定条件下可氧化生成SO3,其主反应为:2SO2(g)+O2(g)?2SO3(g)+Q,若此反应起始的物质的量相同,则各关系图正确的是
a、
 b、
b、
c、
 d、
d、
(4)实际生产用氨水吸收SO2生成亚硫酸的铵盐.现取a克该铵盐,若将其中的SO2全部反应出来,应加入18.4mol/L的硫酸溶液的体积范围为
考点:物质的量或浓度随时间的变化曲线,化学方程式的有关计算
专题:化学平衡专题
分析:(1)a.硫酸常温下,不易分解.
b.反应中二氧化硫表现还原性,氧化性比HI强.
c.1molSO2消耗2molH2O生成1molH2SO4,1molH2SO4分解生成1molSO2与1molH2O.
d.由Ⅲ可知产生lmolO2的同时产生2molSO2,由I可知2molSO2生成4molHI,由Ⅱ可知4molHI分解生成2mol H2.
(2)由图可知,2min内H2物质的量的变化量,然后计算化学反应速率,再利用化学反应速率之比等于化学计量数之比来解答;根据反应方程式写平衡表达式;利用浓度对化学平衡的影响来分析HI的平衡浓度、达到平衡的时间、平衡时H2的体积分数,但温度不变,平衡常数不变;
(3)升高温度,加快反应速率到达平衡的时间缩短,逆反应速率增大更多,平衡向逆反应方向移动,三氧化硫的含量降低;增大压强,加快反应速率到达平均的时间缩短,正反应速率增大更多,平衡向正反应方向移动,二氧化硫的含量减少;使用催化剂,能加快反应速率,缩短达到平衡的时间,但不影响平衡,据此结合图象判断;
(4)二氧化硫和氨水反应可生成亚硫酸铵或亚硫酸氢铵,计算出ag亚硫酸铵或亚硫酸氢铵放出二氧化硫消耗硫酸的体积.
b.反应中二氧化硫表现还原性,氧化性比HI强.
c.1molSO2消耗2molH2O生成1molH2SO4,1molH2SO4分解生成1molSO2与1molH2O.
d.由Ⅲ可知产生lmolO2的同时产生2molSO2,由I可知2molSO2生成4molHI,由Ⅱ可知4molHI分解生成2mol H2.
(2)由图可知,2min内H2物质的量的变化量,然后计算化学反应速率,再利用化学反应速率之比等于化学计量数之比来解答;根据反应方程式写平衡表达式;利用浓度对化学平衡的影响来分析HI的平衡浓度、达到平衡的时间、平衡时H2的体积分数,但温度不变,平衡常数不变;
(3)升高温度,加快反应速率到达平衡的时间缩短,逆反应速率增大更多,平衡向逆反应方向移动,三氧化硫的含量降低;增大压强,加快反应速率到达平均的时间缩短,正反应速率增大更多,平衡向正反应方向移动,二氧化硫的含量减少;使用催化剂,能加快反应速率,缩短达到平衡的时间,但不影响平衡,据此结合图象判断;
(4)二氧化硫和氨水反应可生成亚硫酸铵或亚硫酸氢铵,计算出ag亚硫酸铵或亚硫酸氢铵放出二氧化硫消耗硫酸的体积.
解答:
解:(1)a.硫酸常温下温度,不易分解,故a错误;
b.反应中二氧化硫表现还原性,还原性比HI强,故b正确;
c.1molSO2消耗2molH2O生成1molH2SO4,1molH2SO4分解生成1molSO2与1molH2O,循环中水的量减少,故应补充水,故c正确;
d.由Ⅲ可知产生lmolO2的同时产生2molSO2,由I可知2molSO2生成4molHI,由Ⅱ可知4molHI分解生成2mol H2,即循环过程中产生l mol O2的同时产生2mol H2,故d错误;
故选:bc;
(2)由图可知2min内氢气的物质的量增加了0.1mol,则氢气的浓度为
=0.05mol/L,用氢气表示的化学反应速率为
=0.025mol/(L.min),
由反应中的化学计量数可知v(HI)=0.025mol/(L.min)×2=0.05mol/(L.min);根据方程式可写出平衡常数表达式为:K=
;
对该反应,当温度不变开始加入HI(g)的物质的量是原来的2倍,则温度不变,K不变,故a错;物质的量为原来的2倍,该反应是反应前后气体体积相等的反应,
则反应体系中各物质的浓度都是原来的2倍,故b正确;物质的量增大,则化学反应速率先增大的快,后随浓度的减小,速率增大的程度变小,故c错;
由反应方程式及原来的量与后来的量成正比,则这两种情况下建立的平衡为等效平衡,即平衡时H2的体积分数相同,故d错;
故答案为:0.05mol?L-1?min-1;
;b;
(3)升高温度,加快反应速率到达平均的时间缩短,逆反应速率增大更多,平衡向逆反应方向移动,三氧化硫的含量降低,二氧化硫的含量升高,故a错误,b正确;增大压强,加快反应速率到达平均的时间缩短,正反应速率增大更多,平衡向正反应方向移动,二氧化硫的含量减少,图象与实际不符合,故c错误;使用催化剂,能加快反应速率,缩短达到平衡的时间,但不影响平衡,故d正确;
故选:bd;
(4)设ag亚硫酸铵完全转化为二氧化硫消耗硫酸的体积为x,设ag亚硫酸氢铵完全转化为二氧化硫消耗硫酸的体积为y:
(NH4)2SO3 ~H2SO4
116 1mol
ag 18.4x
=
,解得x=
L
2NH4HSO3 ~H2SO4
198g 1mol
ag 18.4y
=
,解得y=
L,
因氨气和二氧化硫反应可能生成亚硫酸铵或亚硫酸氢铵或为亚硫酸铵和亚硫酸酸氢铵的混合物,故消耗硫酸的范围为:
L~
L,故答案为:
L~
L.
b.反应中二氧化硫表现还原性,还原性比HI强,故b正确;
c.1molSO2消耗2molH2O生成1molH2SO4,1molH2SO4分解生成1molSO2与1molH2O,循环中水的量减少,故应补充水,故c正确;
d.由Ⅲ可知产生lmolO2的同时产生2molSO2,由I可知2molSO2生成4molHI,由Ⅱ可知4molHI分解生成2mol H2,即循环过程中产生l mol O2的同时产生2mol H2,故d错误;
故选:bc;
(2)由图可知2min内氢气的物质的量增加了0.1mol,则氢气的浓度为
| 0.1mol |
| 2L |
| 0.05mol/L |
| 2min |
由反应中的化学计量数可知v(HI)=0.025mol/(L.min)×2=0.05mol/(L.min);根据方程式可写出平衡常数表达式为:K=
| c(H2)?c(I2) |
| c2(HI) |
对该反应,当温度不变开始加入HI(g)的物质的量是原来的2倍,则温度不变,K不变,故a错;物质的量为原来的2倍,该反应是反应前后气体体积相等的反应,
则反应体系中各物质的浓度都是原来的2倍,故b正确;物质的量增大,则化学反应速率先增大的快,后随浓度的减小,速率增大的程度变小,故c错;
由反应方程式及原来的量与后来的量成正比,则这两种情况下建立的平衡为等效平衡,即平衡时H2的体积分数相同,故d错;
故答案为:0.05mol?L-1?min-1;
| c(H2)?c(I2) |
| c2(HI) |
(3)升高温度,加快反应速率到达平均的时间缩短,逆反应速率增大更多,平衡向逆反应方向移动,三氧化硫的含量降低,二氧化硫的含量升高,故a错误,b正确;增大压强,加快反应速率到达平均的时间缩短,正反应速率增大更多,平衡向正反应方向移动,二氧化硫的含量减少,图象与实际不符合,故c错误;使用催化剂,能加快反应速率,缩短达到平衡的时间,但不影响平衡,故d正确;
故选:bd;
(4)设ag亚硫酸铵完全转化为二氧化硫消耗硫酸的体积为x,设ag亚硫酸氢铵完全转化为二氧化硫消耗硫酸的体积为y:
(NH4)2SO3 ~H2SO4
116 1mol
ag 18.4x
| 116g |
| ag |
| 1mol |
| 18.4x |
| a |
| 116×18.4 |
2NH4HSO3 ~H2SO4
198g 1mol
ag 18.4y
| 198g |
| a |
| 1mol |
| 18.4y |
| a |
| 198×18.4 |
因氨气和二氧化硫反应可能生成亚硫酸铵或亚硫酸氢铵或为亚硫酸铵和亚硫酸酸氢铵的混合物,故消耗硫酸的范围为:
| a |
| 116×18.4 |
| a |
| 198×18.4 |
| a |
| 116×18.4 |
| a |
| 198×18.4 |
点评:本题主要考查了反应方程式的分析及计算,反应平衡图象,难度中等.对于图象,要看清图象的含义、拐点、平衡点,结合平衡移动规律进行判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列离子方程式书写正确的是( )
| A、少量的金属铜投入浓硝酸中Cu+4H++2NO3-=Cu2++NO2↑+2H2O |
| B、铝片投入稀盐酸中Al+6H+=Al3++3H2↑ |
| C、氢氧化钡溶液与稀硫酸混合Ba2++SO42-=BaSO4↓ |
| D、氢氧化铝与足量烧碱溶液混合Al(OH)3+OH-=AlO2-+2H2O |
我国赢得2008年第29届夏季奥运会的举办权.为向世界展现一个新的形象,某校同学提出下列建议:①开发新能源,减少化石燃料的燃烧;②开发生产无汞电池;③分类回收垃圾;④提倡使用一次性发泡塑料餐具和塑料袋;⑤提倡使用手帕,减少餐巾纸的使用;⑥提倡不使用含磷洗衣粉.你认为可以采纳的是( )
| A、①②③④⑥ | B、②③④⑤⑥ |
| C、①②③⑤⑥ | D、全部 |
下列说法正确的是( )
| A、二氯甲烷有两种同分异构体 |
| B、苯和苯的同系物均能使高锰酸钾酸性溶液褪色 |
| C、醇发生脱水反应一定生成含C=C双键的化合物 |
| D、一定条件下溴乙烷既能发生取代反应又能发生消去反应 |
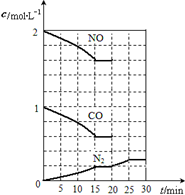 在铂-铑“三效”催化剂作用下,以下反应可以将汽车尾气中2种有
在铂-铑“三效”催化剂作用下,以下反应可以将汽车尾气中2种有