题目内容
 在铂-铑“三效”催化剂作用下,以下反应可以将汽车尾气中2种有
在铂-铑“三效”催化剂作用下,以下反应可以将汽车尾气中2种有害气体转变成无害气体:
2NO(g)+2CO(g)?N2(g)+2CO2(g)+Q(Q>0).
(1)该反应的化学平衡常数表达式为
①加入催化剂 ②降低温度
③缩小容器体积 ④增加CO2的量
(2)铂-铑“三效”催化剂还可帮助将汽车尾气中的烃类转变成无害气体,
生成的无害气体是
(3)有文献报道,在铂-铑“三效”催化剂作用下,280℃时,NOx“转化率”达到90%,这是否指铂-铑“三效”催化剂能移动化学平衡?
(4)等物质的量的NO和CO气体反应时,若NO的转化率为90%,所得混合气体的平均相对分子质量为
考点:物质的量或浓度随时间的变化曲线,化学平衡的影响因素
专题:化学平衡专题
分析:(1)依据方程式和平衡常数概念写出平衡常数表达式;
(2)烃类含C、H元素,烃燃烧生成物是水和二氧化碳;
(3)催化剂不会改变平衡状态,只能缩短达到平衡所用时间;
(4)根据公式平均摩尔质量=
,结合平衡时各组分的量来计算,平均相对分子质量在数值上和摩尔质量相等.
(2)烃类含C、H元素,烃燃烧生成物是水和二氧化碳;
(3)催化剂不会改变平衡状态,只能缩短达到平衡所用时间;
(4)根据公式平均摩尔质量=
| 混合气体总质量 |
| 混合气体总的物质的量 |
解答:
(1)2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0;
平衡常数K=
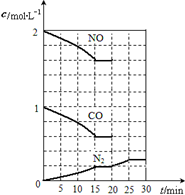
,20min时,若改变反应条件,导致N2浓度发生如图1所示的变化,斜率减小反应速率减小,
氮气浓度增大,正反应是气体体积减小的放热反应,则改变的条件可能是降温,
故答案为:
;②;
(2)烃类含C、H元素,烃燃烧生成物是水和二氧化碳,故答案为:CO2和H2O;
(3)催化剂不会改变平衡状态,只能缩短达到平衡所用时间,故这是铂-铑“三效”催化剂不能移动化学平衡,
三效是指催化效率高,转化速率快,污染排放少;
故答案为:不是;是指催化效率高,NOx转化速率快,排放少;
(4)设起始NO和CO的物质的量为1mol
则 2NO(g)+2CO(g)?N2(g)+2CO2(g)
起始 1 1 0 0
转化 0.9 0.9 0.45 0.9
平衡 0.1 0.1 0.45 0.9
混合气体总质量为:30g+28g=58g,平衡后混合气体总物质的量为:(0.1+0.1+0.45+0.9)mol=1.55mol,
则混合气体的平均摩尔质量为:
=37.42g/mol,故混合气体的平均相对分子质量为37.42,
故答案为;37.42.
平衡常数K=
| c(N2)?c2(CO2) |
| c2(NO)?c2(CO) |
氮气浓度增大,正反应是气体体积减小的放热反应,则改变的条件可能是降温,
故答案为:
| c(N2)?c2(CO2) |
| c2(NO)?c2(CO) |
(2)烃类含C、H元素,烃燃烧生成物是水和二氧化碳,故答案为:CO2和H2O;
(3)催化剂不会改变平衡状态,只能缩短达到平衡所用时间,故这是铂-铑“三效”催化剂不能移动化学平衡,
三效是指催化效率高,转化速率快,污染排放少;
故答案为:不是;是指催化效率高,NOx转化速率快,排放少;
(4)设起始NO和CO的物质的量为1mol
则 2NO(g)+2CO(g)?N2(g)+2CO2(g)
起始 1 1 0 0
转化 0.9 0.9 0.45 0.9
平衡 0.1 0.1 0.45 0.9
混合气体总质量为:30g+28g=58g,平衡后混合气体总物质的量为:(0.1+0.1+0.45+0.9)mol=1.55mol,
则混合气体的平均摩尔质量为:
| 58g |
| 1.55mol |
故答案为;37.42.
点评:本题考查了平衡常数、平衡的移动及平均相对分子质量的计算,难度中等.有关平衡计算,一般按三段式写出起始、转化、平衡量,再根据题目条件进行解答.

练习册系列答案
相关题目
下列反应中,二氧化硫既不是氧化剂又不是还原剂的是( )
| A、SO2+NO2→SO3+NO | ||
| B、SO2+2NaOH→H2O+Na2SO3 | ||
C、SO2+2Mg
| ||
| D、SO2+Br2+2H2O→H2SO4+2HBr |
放射性同位素钬
Ho可有效治疗肝癌.下列关于
Ho的叙述正确的是( )
| 166 |
| 67 |
| 166 |
| 67 |
| A、电子数是166 |
| B、中子数是99 |
| C、质量数是67 |
| D、原子序数是166 |
 如图为番茄电池示意图,其能量转化的主要方式是( )
如图为番茄电池示意图,其能量转化的主要方式是( )| A、化学能转换为电能 |
| B、化学能转换为光能 |
| C、电能转换为化学能 |
| D、光能转换为化学能 |
 分解水制氢气的工业制法之一是硫--碘循环,主要涉及下列反应:
分解水制氢气的工业制法之一是硫--碘循环,主要涉及下列反应: b、
b、
 d、
d、