题目内容
钙在加热时能与氮气、氢气反应.氢化钙遇水立即反应生成氢氧化钙和氢气,氢化钙通常用氢气与金属钙加热制取,图1是横拟制取装置.
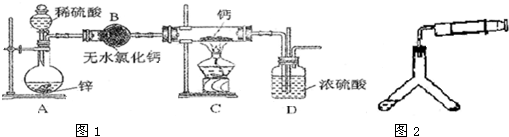
(1)用浓硫酸配制1:4(体积比)的稀硫酸,需用的玻璃仪器是烧杯、 .
(2)装置D中竖直导管的作用是 .
(3)为了确认进入装置C的氢气已经干燥,可在B、C之间再接一装置,该装置中加入的试剂是 .加热C装置前要对H2验纯,方法是:收集一试管气体,将管口靠近酒精灯火焰,若听到“噗噗”的声音,说明H2 .
(4)甲同学认为只要装置合理、操作规范就可以排除生成 (选填序号).
a.Ca3N2 b.CaO c.Ca(OH)2
(5)乙同学用上图2装置测定制得的氢化钙的纯度.他称取46mg样品,与足量水反应,恒温时,注射器量出产生的气体为48.06mL(已换算为标准状况).产生实验误差的原因可能是 (选填编号).
①H2通入不足,反应器中有空气 ②钙与H2未充分反应 ③产物与空气接触
(6)丙同学根据乙同学的实验数据列了一个关系式,42x+40y=0.046、2x+y=
,请指出式子中y的含义 .

(1)用浓硫酸配制1:4(体积比)的稀硫酸,需用的玻璃仪器是烧杯、
(2)装置D中竖直导管的作用是
(3)为了确认进入装置C的氢气已经干燥,可在B、C之间再接一装置,该装置中加入的试剂是
(4)甲同学认为只要装置合理、操作规范就可以排除生成
a.Ca3N2 b.CaO c.Ca(OH)2
(5)乙同学用上图2装置测定制得的氢化钙的纯度.他称取46mg样品,与足量水反应,恒温时,注射器量出产生的气体为48.06mL(已换算为标准状况).产生实验误差的原因可能是
①H2通入不足,反应器中有空气 ②钙与H2未充分反应 ③产物与空气接触
(6)丙同学根据乙同学的实验数据列了一个关系式,42x+40y=0.046、2x+y=
| 48.06 |
| 22400 |
考点:制备实验方案的设计,实验装置综合
专题:实验设计题
分析:(1)利用浓硫酸配制体积比为1:4的稀硫酸,需要用量筒量取浓硫酸1体积,把浓硫酸沿烧杯内壁缓缓注入4体积蒸馏水中并不断搅拌溶解得到,依据操作过程分析需要的玻璃仪器;
(2)装置D中的竖直玻璃管是起到平衡压强的作用;
(3)确认进入装置C的氢气已经干燥,可在B、C之间再接一装置干燥管,利用干燥管中的无水硫酸铜遇到水是否变蓝色,证明氢气是否已经干燥;依据氢气的验纯方法分析判断;
(4)钙在加热时能与氮气、氢气反应.氢化钙遇水立即反应生成氢氧化钙和氢气,上述装置制备过程中先利用生成的氢气充满整套装置,在最后收集验纯,所以装置中无空气存在,不会生成氮化钙,无水蒸气存在,不会生成氢氧化钙和氧化钙;
(5)分析可知装置操作中产生误差的原因可能为装置中H2通入不足,反应器中有空气,钙与H2未充分反应等分析判断;
(2)装置D中的竖直玻璃管是起到平衡压强的作用;
(3)确认进入装置C的氢气已经干燥,可在B、C之间再接一装置干燥管,利用干燥管中的无水硫酸铜遇到水是否变蓝色,证明氢气是否已经干燥;依据氢气的验纯方法分析判断;
(4)钙在加热时能与氮气、氢气反应.氢化钙遇水立即反应生成氢氧化钙和氢气,上述装置制备过程中先利用生成的氢气充满整套装置,在最后收集验纯,所以装置中无空气存在,不会生成氮化钙,无水蒸气存在,不会生成氢氧化钙和氧化钙;
(5)分析可知装置操作中产生误差的原因可能为装置中H2通入不足,反应器中有空气,钙与H2未充分反应等分析判断;
解答:
解:(1)利用浓硫酸配制体积比为1:4的稀硫酸,需要用量筒量取浓硫酸1体积,把浓硫酸沿烧杯内壁缓缓注入4体积蒸馏水中并不断搅拌溶解得到,依据操作过程分析需要的玻璃仪器为烧杯、玻璃棒、量筒;
故答案为:玻璃棒、量筒;
(2)装置D中的竖直玻璃管是起到平衡压强的作用,可以防止液体倒流;
故答案为:平衡压强,防止液体倒流;
(3)确认进入装置C的氢气已经干燥,可在B、C之间再接一装置干燥管,利用干燥管中的无水硫酸铜遇到水是否变蓝色,证明氢气是否已经干燥;依据氢气的验纯方法是收集一试管气体,将管口靠近酒精灯火焰,若听到“噗噗”的声音,说明H2已经纯净;
故答案为:无水硫酸铜;纯净;
(4)钙在加热时能与氮气、氢气反应.氢化钙遇水立即反应生成氢氧化钙和氢气,上述装置制备过程中先利用生成的氢气充满整套装置,在最后收集验纯,所以装置中无空气存在,不会生成氮化钙,无水蒸气存在,不会生成氢氧化钙和氧化钙;
故答案为:abc;
(5)分析可知装置操作中产生误差的原因可能为装置中H2通入不足,反应器中有空气,钙与H2未充分反应,导致氢化钙质量减小,都可以造成实验误差,产物与空气接触不影响纯度的测定,依据的是钙元素守恒和生成氢气的体积计算得到;
故答案为:①②;
(6)丙同学根据乙同学的实验数据列了一个关系式,42x+40y=0.046、2x+y=
,依据质量关系式,摩尔质量大小分析可知,X为氢化钙物质的量,式子中y的含义为钙的物质的量;
故答案为:钙的物质的量;
故答案为:玻璃棒、量筒;
(2)装置D中的竖直玻璃管是起到平衡压强的作用,可以防止液体倒流;
故答案为:平衡压强,防止液体倒流;
(3)确认进入装置C的氢气已经干燥,可在B、C之间再接一装置干燥管,利用干燥管中的无水硫酸铜遇到水是否变蓝色,证明氢气是否已经干燥;依据氢气的验纯方法是收集一试管气体,将管口靠近酒精灯火焰,若听到“噗噗”的声音,说明H2已经纯净;
故答案为:无水硫酸铜;纯净;
(4)钙在加热时能与氮气、氢气反应.氢化钙遇水立即反应生成氢氧化钙和氢气,上述装置制备过程中先利用生成的氢气充满整套装置,在最后收集验纯,所以装置中无空气存在,不会生成氮化钙,无水蒸气存在,不会生成氢氧化钙和氧化钙;
故答案为:abc;
(5)分析可知装置操作中产生误差的原因可能为装置中H2通入不足,反应器中有空气,钙与H2未充分反应,导致氢化钙质量减小,都可以造成实验误差,产物与空气接触不影响纯度的测定,依据的是钙元素守恒和生成氢气的体积计算得到;
故答案为:①②;
(6)丙同学根据乙同学的实验数据列了一个关系式,42x+40y=0.046、2x+y=
| 48.06 |
| 22400 |
故答案为:钙的物质的量;
点评:本题考查了制备实验的过程分析,溶液配制方法和过程应用,主要是我在制备注意问题和物质性质的分析判断,题干信息应用是解题关键,题目难度较大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
 下列关于如图所示装置的叙述,正确的是(水果电池示意图)( )
下列关于如图所示装置的叙述,正确的是(水果电池示意图)( )| A、铜是负极 |
| B、电能转变为化学能 |
| C、电子从铜片经导线流向锌片 |
| D、水果汁起到导电作用 |
在加热时,浓硫酸与铜发生反应的化学方程式为:2H2SO4(浓)+Cu
CuSO4+SO2↑+2H2O对于该反应,下列说法中不正确的是( )
| ||
| A、是氧化还原反应 |
| B、铜是还原剂 |
| C、H2SO4表现了氧化性和酸性 |
| D、反应后铜元素的化合价降低 |
下列有关实验室制取气体的反应中,不属于氧化还原反应的是( )
| A、用稀硫酸和锌粒制氢气 |
| B、用氯酸钾和二氧化锰加热制氧气 |
| C、用浓盐酸和漂白粉共热制氯气 |
| D、用石灰石和稀盐酸制二氧化碳 |
 分解水制氢气的工业制法之一是硫--碘循环,主要涉及下列反应:
分解水制氢气的工业制法之一是硫--碘循环,主要涉及下列反应: b、
b、
 d、
d、