题目内容
7.下列物质,是强电解质的是( )| A. | 硫酸钠 | B. | 石墨 | C. | 稀H2SO4 | D. | CO2 |
分析 在水溶液中或熔融状态下能完全电离的化合物为强电解质,据此分析.
解答 解:A、硫酸钠在水溶液中和熔融状态下均能完全电离,故为强电解质,故A正确;
B、石墨是单质,既不是电解质也不是非电解质,故B错误;
C、稀硫酸是混合物,既不是电解质也不是非电解质,更不是强电解质,故C错误;
D、二氧化碳在水溶液中和熔融状态下均不能导电,故为非电解质,故D错误.
故选A.
点评 本题考查了强电解质的概念,化合物分为电解质和非电解质,电解质根据能否完全电离又分为强电解质和弱电解质,难度不大,注意基础的掌握.

练习册系列答案
相关题目
17.下列过程不属于氮的固定的是( )
| A. | 工业合成氨 | B. | 工业上用氨催化氧化法制备硝酸 | ||
| C. | 闪电导致雷雨中含有硝酸 | D. | 豆科植物的根瘤菌制造含氮化合物 |
18. 甲~辛等元素在周期表中的相对位置如下表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如下表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
 甲~辛等元素在周期表中的相对位置如下表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如下表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )| A. | 丙与庚的原子核外电子数相差3 | |
| B. | 原子半径:辛>己>戊 | |
| C. | 金属性:甲>乙>丁 | |
| D. | 乙的单质在空气中燃烧生成只含离子键的化合物 |
15.下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1 CH3COOH溶液与0.1 mol•L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)>c(CH3COO-) | |
| B. | 10 mL 0.1 mol•L-1 CH3COONa溶液与10 mL 0.1 mol•L-1 CH3COOH溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 0.1 mol•L-1 NaHCO3溶液与0.1 mol•L-1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) |
12.利用下列装置(部分仪器已省略),能顺利完成对应实验的是( )
| A. | 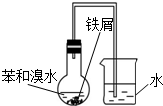 实验室制取溴苯 | B. | 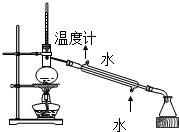 石油的分馏实验 | ||
| C. | 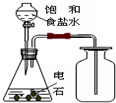 实验室制取乙炔并收集 | D. |  利用酒精萃取碘水中的I2单质 |
19.下列实验,能获得成功的是( )
| A. | 用溴水鉴别苯、乙醇、苯乙烯 | |
| B. | 苯、溴水、铁粉混合制溴苯 | |
| C. | 用分液漏斗分离苯和乙醇 | |
| D. | 加浓溴水,然后过滤除去苯中混有的少量己烯 |
16.除去下列物质中的杂质(括号内为杂质),所选用的试剂不正确的一组是( )
| 选项 | 待提纯的物质 | 选用的试剂 |
| A | N2(O2) | 灼热的铜网 |
| B | SO2(SO3) | 饱和Na2SO3溶液 |
| C | H2(H2S) | CuSO4溶液 |
| D | CO2(SO2) | 酸性KMnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |