题目内容
4.将足量的稀盐酸加到由下列物质组成的固体混合物中,只能发生一种类型反应的是( )| A. | Al、Cu、AgNO3 | B. | Na2O2、Na2SO3、BaCl2 | ||
| C. | CaCO3、Na2SiO3、CH3COONa | D. | Ba(NO3)2、Fe(OH)2、NaOH |
分析 盐酸具有酸性,可发生中和反应,与活泼金属发生置换反应,盐、碱性氧化物发生复分解反应,以此解答该题.
解答 解:A.Al与盐酸反应生成氢气和氯化铝,为置换反应,硝酸银与盐酸反应生成沉淀,发生复分解反应,故A不选;
B.过氧化钠与盐酸反应生成氧气和氯化钠,为氧化还原反应,盐酸与亚硫酸钠反应生成二氧化硫气体,为复分解反应,故B不选;
C.盐酸与CaCO3、Na2SiO3、CH3COONa发生复分解反应,故C选;
D.盐酸与硝酸钡溶液不反应,与氢氧化亚铁、氢氧化钠发生中和反应,故D不选.
故选C.
点评 本题考查元素单质及化合物的性质,为高频考点,侧重于学生的分析能力的考查,题目涉及的物质较多,熟练掌握物质的性质是关键,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
6.下列关于物质检验或鉴别的说法错误的是( )
| A. | 用CCl4鉴别溴水和碘水 | |
| B. | 用AgNO3溶液鉴别溴化钾溶液和氯化钠溶液 | |
| C. | 向某盐溶液中加入氢氧化钠溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,溶液中一定有NH4+ | |
| D. | 向某盐溶液中,加入盐酸,产生使澄清石灰水变浑浊的气体,溶液中含有大量CO32-离子 |
13.下面是一些常见分子的比例模型.其中1个分子中含有共用电子对最多的是( )
| A. |  氢气 | B. |  氨气 | C. |  水 | D. |  二氧化碳 |
14.下列关于反应中能量变化说法正确的是( )
| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O (g)△H=-890.3 kJ•mol-1 | |
| B. | 相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | |
| C. | 常温下,反应C(s)+CO2(g)═2CO(g) 不能自发进行,则该反应的△H<0 | |
| D. | 已知①2H2(g)+O2(g)═2H2O (g)△H1=a kJ•mol-1②2H2(g)+O2(g)═2H2O (l)△H2=b kJ•mol-1,则a>b |
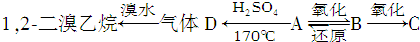 若有A、B、C三种烃的衍生物,相互转化关系如图:C跟石灰石反应产生使石灰水变浑浊的气体.
若有A、B、C三种烃的衍生物,相互转化关系如图:C跟石灰石反应产生使石灰水变浑浊的气体.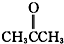 酮类 ③CH3CH2Br卤代烃
酮类 ③CH3CH2Br卤代烃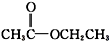 酯类 ⑤
酯类 ⑤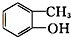 酚类 ⑥
酚类 ⑥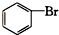 卤代烃
卤代烃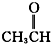 醛类 ⑧
醛类 ⑧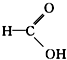 羧酸类 ⑨
羧酸类 ⑨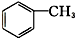 芳香烃.
芳香烃.