题目内容
6.下列试剂在空气中久置因为O2而变质的是( )| A. | Na2O2 | B. | Ca( ClO)2 | C. | FeSO4 | D. | 浓盐酸 |
分析 试剂在空气中久置因为O2而变质,说明该物质具有较强的还原性,能被空气中的氧气氧化,以此解答该题.
解答 解:A.过氧化钠与空气中二氧化碳、水发生反应而变质,故A错误;
B.次氯酸钙与空气中二氧化碳、水发生反应而变质,故B错误;
C.硫酸亚铁具有还原性,易被氧化而变质,故C正确;
D.浓盐酸易挥发,与氧气不反应,故D错误.
故选C.
点评 本题考查学生物质的性质以及氧化还原反应的概念和判断,侧重于常见物质的性质的考查,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
16.国际理论与应用化学联合会(IUPAC)2012年5月正式确认了114号和116号元素并宣布其名称,其中关于${\;}_{116}^{292}$Lv的说法正确的是( )
| A. | 质量数为292 | B. | 中子数为116 | C. | 电子数为292 | D. | 质子数为176 |
1.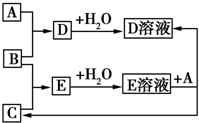 已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.下列说法中不正确的是( )
已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.下列说法中不正确的是( )
 已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.下列说法中不正确的是( )
已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.下列说法中不正确的是( )| A. | A、B、C中三种元素的任意两种元素形成的化合物所属物质类别可能是氧化物 | |
| B. | A、B、C中三种元素形成的化合物所属物质类别一定不是碱 | |
| C. | 如果E溶液是一种强酸,则E溶液为盐酸 | |
| D. | A、B、C中有一种金属且为A |
18.下列化学用语表示正确的是( )
| A. | N2分子的电子式: | B. | 乙醇的结构简式:C2H6O | ||
| C. | 镁离子的结构示意图: | D. | CO2的比例模型: |
15.下列物质的属类归纳中不正确的是( )
| A. | 蔗糖、酒精、甲烷等含碳化合物称为有机物 | |
| B. | 由金属离子和酸根离子组成的化合物称为盐 | |
| C. | 在水溶液中电离出的阳离子全部为氢离子的化合物 | |
| D. | 含氧元素的化合物称为氧化物 |
3.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是BC(多选扣分).
A.容器中压强不变 B.混合气体中 c(CO)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)某温度下,将CO和水蒸气各1mol置于体积为1L的密闭容器中反应,达到平衡后测得CO2为0.5mol,再通入4mol水蒸气,达到新的平衡后CO2的物质的量等于$\frac{5}{6}$mol.
其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是BC(多选扣分).
A.容器中压强不变 B.混合气体中 c(CO)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)某温度下,将CO和水蒸气各1mol置于体积为1L的密闭容器中反应,达到平衡后测得CO2为0.5mol,再通入4mol水蒸气,达到新的平衡后CO2的物质的量等于$\frac{5}{6}$mol.

 +2nH2O.
+2nH2O.