题目内容
(1)3.6克H2O的物质的量是 ,含有 个H2O,含有 molH.
(2)在同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为 ,物质的量之比为 ,原子总数之比为 ;质量之比为 .
(3)在标准状况下,22g CO2气体的体积是 L,与 g N2含有相同的分子数.
(2)在同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为
(3)在标准状况下,22g CO2气体的体积是
考点:物质的量的相关计算
专题:计算题
分析:结合n=
、n=
、N=nNA及分子构成计算.
| m |
| M |
| V |
| Vm |
解答:
解:(1)3.6克H2O的物质的量是
=0.2mol,含0.2mol×NA=1.204×1023个H2O,含有n(H)=0.2mol×2=0.4mol,
故答案为:0.2mol;1.204×1023;0.4;
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳,物质的量相同,由N=nNA可知,分子数相同之比为1:1,物质的量之比为1:1,原子总数之比为1×5:1×3=5:3,质量比为1×16:1×44=4:11,
故答案为:1:1;1:1;5:3;4:11;
(3)标准状况下,22g CO2气体的体积是
×22.4L/mol=11.2L,物质的量为0.5mol,则0.5molN2的质量为0.5mol×28g/mol=14g,二者分子数相同,
故答案为:11.2;14.
| 3.6g |
| 18g/mol |
故答案为:0.2mol;1.204×1023;0.4;
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳,物质的量相同,由N=nNA可知,分子数相同之比为1:1,物质的量之比为1:1,原子总数之比为1×5:1×3=5:3,质量比为1×16:1×44=4:11,
故答案为:1:1;1:1;5:3;4:11;
(3)标准状况下,22g CO2气体的体积是
| 22g |
| 44g/mol |
故答案为:11.2;14.
点评:本题考查物质的量的计算,为高频考点,把握以物质的量为中心的基本计算公式为解答的关键,侧重分析与计算能力的综合考查,题目难度不大.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
下列说法中正确的是( )
| A、在101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热 |
| B、酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
| C、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| D、由单质A转化为单质B,△H=+119KJ/mol,可知单质A比单质B稳定 |
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是( )
A、 腐蚀品 |
B、 爆炸品 |
C、 有毒气体 |
D、 易燃液体 |
 最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量.则下列说法正确的是( )
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量.则下列说法正确的是( )| A、N4属于一种新型的化合物 |
| B、1mo1N4气体转变为N2将放出882kJ热量 |
| C、N4与N2互为同分异构体 |
| D、N4沸点比P4(白磷)沸点高 |
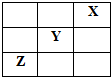 X、Y、Z是Ⅳ~ⅦA族的三种非金属元素,它们在周期表中的位置如图所示.试回答:
X、Y、Z是Ⅳ~ⅦA族的三种非金属元素,它们在周期表中的位置如图所示.试回答: