题目内容
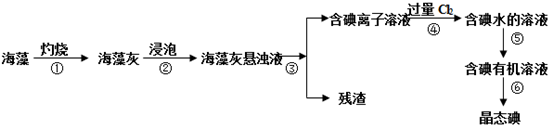
碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素.在实验室中,从海藻里提取碘的流程和实验装置如下:
(1)指出上述提取碘的过程中有关实验操作的名称:步骤③ ,步骤⑤ .
(2)写出步骤④对应反应的离子方程式: .
(3)提取碘的过程中,可供选择的有机试剂是 .(填编号)
A.酒精 B.醋酸 C.四氯化碳 D.苯
(4)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是 .
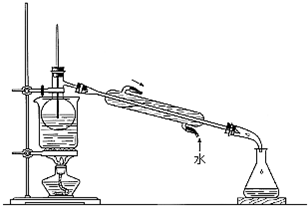
(5)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏.指出下图实验装置中存在的错误之处: .

(1)指出上述提取碘的过程中有关实验操作的名称:步骤③
(2)写出步骤④对应反应的离子方程式:
(3)提取碘的过程中,可供选择的有机试剂是
A.酒精 B.醋酸 C.四氯化碳 D.苯
(4)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是
(5)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏.指出下图实验装置中存在的错误之处:

考点:海水资源及其综合利用
专题:实验设计题
分析:海藻在坩埚中灼烧得到海藻灰,将海藻灰浸泡得到海藻灰悬浊液,然后利用过滤的方法分离海藻灰悬浊液,得到残渣和溶液,在溶液中通入过量氯气,氯气和碘离子发生氧化还原反应得失I2,向含有I2的溶液中加入有机溶剂进行萃取,得到含有碘的有机溶液,再利用蒸馏的方法得到晶态碘,再结合题目分析解答.
解答:
解:海藻在坩埚中灼烧得到海藻灰,将海藻灰浸泡得到海藻灰悬浊液,然后利用过滤的方法分离海藻灰悬浊液,得到残渣和溶液,在溶液中通入过量氯气,氯气和碘离子发生氧化还原反应得失I2,向含有I2的溶液中加入有机溶剂进行萃取,得到含有碘的有机溶液,再利用蒸馏的方法得到晶态碘,
(1)分离不溶性固体和溶液采用过滤方法,分离碘水中的碘采用萃取的方法,所以③是过滤、⑤是萃取,
故答案为:过滤;萃取;
(2)氯气具有强氧化性,能将碘离子氧化为碘,离子方程式为Cl2+2I-═I2+2Cl-,故答案为:Cl2+2I-═I2+2Cl-;
(3)萃取剂的选取标准:萃取剂和溶质不反应,萃取剂和原溶剂不互溶,溶质在萃取剂中的溶解度大于在原溶剂中的溶解度,
A.酒精和水互溶,所以不能作萃取剂,故A错误;
B.醋酸和水互溶,所以不能作萃取剂,故B错误;
C.四氯化碳符合萃取剂的选取条件,所以可作萃取剂,故C正确;
D.苯符合萃取剂的选取条件,所以可作萃取剂,故D正确;
故答案为:CD.
(4)③缺少用于过滤的普通漏斗、⑤缺少用于萃取使用的分液漏斗,故答案为:普通漏斗;分液漏斗;
(5)蒸馏时,温度计测量馏分的温度,所以温度计水银球应该位于蒸馏烧瓶支管口处,故答案为:温度计水银球的位置不对.
(1)分离不溶性固体和溶液采用过滤方法,分离碘水中的碘采用萃取的方法,所以③是过滤、⑤是萃取,
故答案为:过滤;萃取;
(2)氯气具有强氧化性,能将碘离子氧化为碘,离子方程式为Cl2+2I-═I2+2Cl-,故答案为:Cl2+2I-═I2+2Cl-;
(3)萃取剂的选取标准:萃取剂和溶质不反应,萃取剂和原溶剂不互溶,溶质在萃取剂中的溶解度大于在原溶剂中的溶解度,
A.酒精和水互溶,所以不能作萃取剂,故A错误;
B.醋酸和水互溶,所以不能作萃取剂,故B错误;
C.四氯化碳符合萃取剂的选取条件,所以可作萃取剂,故C正确;
D.苯符合萃取剂的选取条件,所以可作萃取剂,故D正确;
故答案为:CD.
(4)③缺少用于过滤的普通漏斗、⑤缺少用于萃取使用的分液漏斗,故答案为:普通漏斗;分液漏斗;
(5)蒸馏时,温度计测量馏分的温度,所以温度计水银球应该位于蒸馏烧瓶支管口处,故答案为:温度计水银球的位置不对.
点评:本题考查了海水资源的综合利用,从整体上把握碘的制取,知道每一步可能发生的反应及其相应的操作,知道每一步操作中需要的仪器,知道萃取剂的选取方法,题目难度不大.

练习册系列答案
相关题目
当2NO2(g)?N2O4(g)反应达平衡后,保持其它条件不变,压缩混合气体体积,所观察到的现象是( )
| A、红棕色先变浅后变深最终颜色较浅 |
| B、红棕色先变浅后变深最终颜色较深 |
| C、红棕色先变深后再变浅最终颜色较浅 |
| D、红棕色先变深后变浅最终颜色较深 |
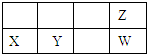
四种短周期元素在周期表中的位置如图,其中Y元素被称为“国防金属”.下列说法不正确是( )

A、X离子结构示意图: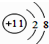 |
| B、原子半径Y比Z大 |
| C、元素的气态氢化物的稳定性Z强于W |
| D、X和Y两元素的最高价氧化物的对应水化物能相互反应 |
下列实验操作中,所用仪器合理的是( )
| A、用托盘天平称取25.20gNaCl |
| B、用四氯化碳萃取碘的饱和水溶液中的碘分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出. |
| C、在蒸发皿中放入NaCl溶液,加热、蒸发制取NaCl晶体 |
| D、用100mL容量瓶配制50mL0.1mol/L的盐酸 |
一小块钠置于空气中,有下列现象:①变成白色粉末,②变暗,③变成白色固体,④变成液体,上述现象出现的先后顺序是 ( )
| A、①②③④ | B、②③④① |
| C、②③①④ | D、③②④① |
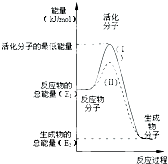 (1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图,然后回答问题.
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图,然后回答问题.