题目内容
12. A、B、C三种固体物质的溶解度曲线如图所示.
A、B、C三种固体物质的溶解度曲线如图所示.(1)t1℃时,A、B、C的溶解度大小关系是B>A=C(用“>”、“<”或“=”表示),它们的饱和溶液中,溶质质量分数最大的物质是B;
(2)t2℃时,将A、B、C各25g分别放入100g水中,能形成饱和溶液的物质是C,将其转化为不饱和溶液的方法有降低温度、增加溶剂.
分析 溶解度的概念是在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的溶质的质量,叫做这种物质在这种溶剂中的溶解度.
(1)由图可知在t1℃时,A与C的溶解度都为25g,则溶解度相等,B的溶解度为40g,则B的溶解度最大;在相同温度,溶解度越大,饱和溶液的溶质质量分数越大;
(2)t1℃时,25gC在100g水中已是饱和溶液,C的溶解度随温度升高而降低,则t2℃时,C有晶体析出,仍是饱和溶液;A、B的溶解度随温度升高而增大,转化为不饱和溶液的方法有降低温度、增加溶剂.
解答 解:溶解度的概念是在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的溶质的质量,叫做这种物质在这种溶剂中的溶解度.
(1)由图可知在t1℃时,A与C的溶解度都为25g,则溶解度相等,B的溶解度为40g,则B的溶解度最大;在相同温度,溶解度越大,饱和溶液的溶质质量分数越大;
故答案为:B>A=C;B;
(2)t1℃时,25gA和C分别在100g水中已是饱和溶液,B未达饱和,从图中得出A、B的溶解度随温度升高而增大,C的溶解度随温度升高而降低,则t2℃时,C有晶体析出,仍是饱和溶液,A、B是不饱和溶液;A、B的溶解度随温度升高而增大,转化为不饱和溶液的方法有降低温度、增加溶剂,
故答案为:C;降低温度;增加溶剂.
点评 本题考查溶解度曲线表示的意义及固体溶解度的概念,培养学生对概念的理解能力和应用能力,难度中等.

练习册系列答案
相关题目
8.为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2,CO2,SO2,NO,CO,不考虑其他成分),设计了如下流程: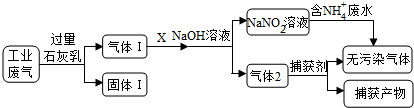
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 固体Ⅰ中主要含有Ca(OH)2、CaCO3、CaSO3 | |
| B. | X可以是空气,且需过量 | |
| C. | 捕获剂所捕获的气体主要是CO | |
| D. | 处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-=N2↑+2H2O |
17.下列物质不能导电但属于电解质的是( )
| A. | 熔融的氯化镁 | B. | 饱和食盐水 | C. | 固态二氧化碳 | D. | 液态氯化氢 |
4.四种仪器中,不能用来加热的是( )
| A. |  | B. |  | C. |  | D. |  |
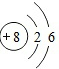 ;
; ;
; ,X属于共价化合物.
,X属于共价化合物. .
.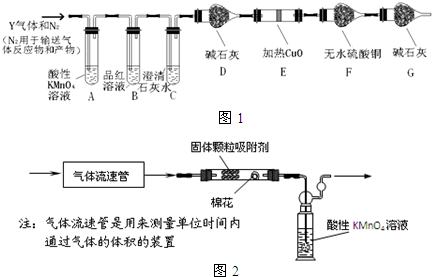
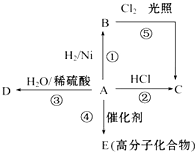 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.根据图回答下列问题:
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.根据图回答下列问题: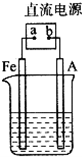 某地区常下酸雨,因而使金属制品锈蚀严重,铁制品镀铜可以有效防止铁的锈蚀,右图所示为铁制品镀铜的过程,请据此回答下列问题:
某地区常下酸雨,因而使金属制品锈蚀严重,铁制品镀铜可以有效防止铁的锈蚀,右图所示为铁制品镀铜的过程,请据此回答下列问题: