题目内容
5.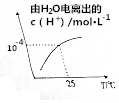 某溶液中由水电离出的c(H+)随温度的变化如图所示,则该溶液可能为( )
某溶液中由水电离出的c(H+)随温度的变化如图所示,则该溶液可能为( )| A. | 稀硫酸 | B. | NaCl溶液 | C. | NH4NO3溶液 | D. | Ba(OH)2溶液 |
分析 根据图示可知,在25℃时,水电离出的氢离子浓度为10-4mol/L,即水的电离被促进.而在酸溶液和碱溶液中,水的电离均被抑制,在盐溶液中,水的电离被促进,据此分析.
解答 解:根据图示可知,在25℃时,水电离出的氢离子浓度为10-4mol/L,即水的电离被促进.
A、酸对水的电离有抑制作用,故A错误;
B、氯化钠是强酸强碱盐,不水解,对水的电离无影响,故B错误;
C、硝酸铵是强酸弱碱盐,在溶液中水解,对水的电离有促进作用,故C正确;
D、氢氧化钡是强碱,对水的电离有抑制作用,故D错误.
故选C.
点评 本题考查了溶液中水的电离程度,应注意的是酸和碱对水的电离均由抑制作用,而盐的水解对水的电离有促进作用.

练习册系列答案
相关题目
7.下列实验操作完全正确的是( )
| 编号 | 实验 | 操作 |
| A | 钠与水的反应 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 制取Fe(OH)3胶体 | 往盛有沸水的烧杯中滴加饱和FeCl3溶液,继续煮沸并用玻璃棒不断搅拌 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体分液漏斗上端管口倒出 |
| A. | A | B. | B | C. | C | D. | D |
13.某溶液中只可能含有下列离子中的某几种:K+、NH4+、Ba2+、SO42-、I-、AlO2-,分别取样:①用pH计测试,溶液显弱酸性;②加氯水和CCl4振荡后静置,下层呈无色.为确定该溶液的组成,还需检验的离子是( )
| A. | Ba2+ | B. | SO42- | C. | K+ | D. | NH4+ |
10.有关热稳定性强弱的比较,不正确的是( )
| A. | KClO3<KCl | B. | K2MnO4>KMnO4 | C. | NaHCO3>Na2CO3 | D. | CaCO3<CaO |
14.只改变一个条件,则下列对图象的解读正确的是( )
| A. | 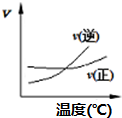 A2(g)+3B2(g)?2AB3(g)如图说明此反应的正反应是吸热反应 | |
| B. | 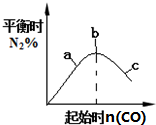 4CO(g)+2NO2(g)?N2(g)+4CO2(g)如图说明NO2的转化率b>a>c | |
| C. | 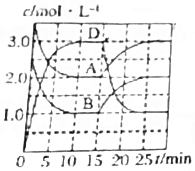 A(g)+B(g)?C(s)+2D(g)△H>0如说明反应至15min时,改变的条件是升高温度 | |
| D. | 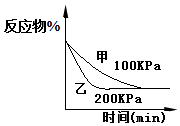 2A(g)+2B(g)?3C(g)+D(?)如图说明生成物D一定是气体 |
15.图为锌一铜原电池示意图,下列说法错误的是( )
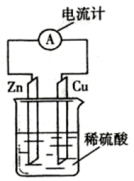

| A. | 电子由铜片通过导线流向锌片 | |
| B. | 锌片为负极,且锌片逐渐浓解 | |
| C. | 铜为正极,铜不易失电了而受到保护 | |
| D. | 该装置能将化学能抟变为电能 |
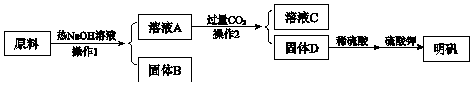
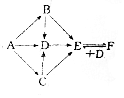 有A、B、C、D、E、F六种物质,其中A是金属单质,灼烧时火焰呈黄色,C为淡黄色固体,其他均为白色固体,它们之间的相互转化关系如图所示(反应条件及其他产物均已略去).
有A、B、C、D、E、F六种物质,其中A是金属单质,灼烧时火焰呈黄色,C为淡黄色固体,其他均为白色固体,它们之间的相互转化关系如图所示(反应条件及其他产物均已略去).