题目内容
某氧化物的化学式为R2O3,电子总数为50,已知氧原子核内有8个中子,R2O3的相对分子质量为102,则R原子核内中子数为
A.10 B.12 C.14 D.21
C
【解析】
试题分析:O是8号元素,原子核内有8个质子,氧原子核内有8个中子,所以O原子的相对原子质量是16,由于R2O3的相对分子质量为102,所以R的相对原子质量是(102-3×16)÷2=27,由于R2O3的电子总数为50,所以R的质子数是(50-3×8)÷2=13,故R原子核内中子数为27—13=14,故选项是C。
考点:考查元素原子的相对原子质量、化合物的电子的关系的知识。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
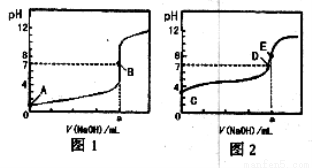

 H++OH- △H>0。下列叙述正确的是
H++OH- △H>0。下列叙述正确的是