题目内容
对于0.1 mol·L-1Na2SO3溶液,正确的是
A.升高温度,溶液pH降低
B.c(Na+)=2c(SO32—)+c(HSO3—)+c(H2SO3)
C.c(Na+)+c(H+)=2c(SO32—)+2c(HSO3—)+c(OH-)
D.加入少量NaOH固体,c(SO32—)与c(Na+)均增大
D
【解析】
试题分析:A.Na2SO3是强碱弱酸盐,水解使溶液显碱性。由于水解反应是吸热反应,所以升高温度会促进盐的水解,溶液pH增大,错误;B.根据物料守恒可得c(Na+)=2c(SO32—)+2c(HSO3—)+2c(H2SO3),错误;C.根据电荷守恒可得c(Na+)+c(H+)=2c(SO32—)+c(HSO3—)+c(OH-),错误;D.加入少量NaOH固体,c(Na+)增大,由于c(OH-)增大,使水解平衡SO32—+ H2O HSO3—+ OH-逆向移动,所以c(SO32—)增大,正确。
HSO3—+ OH-逆向移动,所以c(SO32—)增大,正确。
考点:考查电解质溶液的酸碱性及溶液中离子浓度的大小比较的知识。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
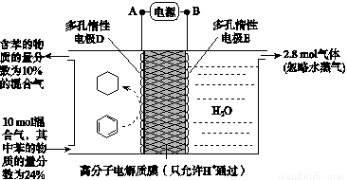
 ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)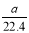 mo1·L-1 B.
mo1·L-1 B.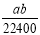 mol·L-1
mol·L-1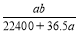 mol·L-1 D.
mol·L-1 D.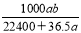 mol·L-1
mol·L-1