题目内容
6.二氧化硫是引起酸雨的一种物质,二氧化硫属于( )| A. | 电解质 | B. | 酸性氧化物 | C. | 含氧酸 | D. | 混合物 |
分析 A.按照物质的组成对物质进行分类,水溶液中或熔融状态下导电的化合物为电解质,水溶液中和熔融状态下都不导电的化合物为非电解质;
B.二氧化硫是氧化物与碱溶液反应生成盐和水,为酸性氧化物;
C.酸根离子含氧元素的酸为含氧酸,水溶液中电离出的阳离子全部是氢离子的化合物为酸;
D.混合物是有不同种物质组成.
解答 解:A.二氧化硫在水溶液中和水反应生成了电解质亚硫酸,二氧化硫本身不能电离出离子属于非电解质,故A错误;
B.酸性氧化物是指氧化物与碱溶液反应生成盐和水的化合物,二氧化硫和碱溶液反应生成盐和水属于酸性氧化物,故B正确;
C.二氧化硫本身不能电离,组成分析属于氧化物,不是含氧酸,故C错误;
D.二氧化硫是一种物质组成属于纯净物,故D错误.
故选B.
点评 本题主要考查基本概念的准确把握,主要是物质分类、物质组成,掌握基础是解题关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下:

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
请问答下列问题:
(1)酸浸前将碳酸锰矿粉碎的作用是增大接触面积,加快反应速率(使反应更充分).
(2)酸浸后的溶液中含有Mn2+、SO42-,另含有少量Fe2+、Fe3+、Al3+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其离子反应方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
②加入CaO将溶液的pH调到5.2~6.0,其主要目的除去Fe3+,A13+.
③加入BaS,除去Cu2+、Pb2+.

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Pb(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 8.0 | 8.3 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.8 | 9.8 |
(1)酸浸前将碳酸锰矿粉碎的作用是增大接触面积,加快反应速率(使反应更充分).
(2)酸浸后的溶液中含有Mn2+、SO42-,另含有少量Fe2+、Fe3+、Al3+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其离子反应方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
②加入CaO将溶液的pH调到5.2~6.0,其主要目的除去Fe3+,A13+.
③加入BaS,除去Cu2+、Pb2+.
17.一定条件下,向2L密闭容器中加入2molN2和10molH2,发生反应N2(g)+3H2(g)?2NH3(g).2min时测得剩余N2为1mol,此时表示的化学反应速率正确的是( )
| A. | v(N2)=0.25mol•L-1•min-1 | B. | v(H2)=0.5mol•L-1•min-1 | ||
| C. | v(NH3)=1mol•L-1•min-1 | D. | v(NH3)=0.25mol•L-1•min-1 |
1.表为周期表中短周期的一部分,若R元素的最高正价和最低负价的绝对值之差为2,则说法正确的是( )
| R | ||
| X | Y | Z |
| A. | 原子半径大小顺序是:Y>X>R | |
| B. | 其气态氢化物的稳定性顺序是:Z>Y>X>R | |
| C. | X、Y、Z中Z的氧化物对应的水化物的酸性最强 | |
| D. | R的气态氢化物与它的含氧酸之间能发生化学反应 |
11.下列说法正确的是( )
| A. | NH3可以用来做喷泉实验是因为其有特殊气味 | |
| B. | 工业上用氨和二氧化碳合成尿素属于氮的固定 | |
| C. | 液氨作制冷剂原因是其气化时大量吸收周围的热量 | |
| D. | NH3能使无色酚酞溶液变红 |
15.下列用水就能鉴别的一组物质是( )
| A. | 苯、己烷、四氯化碳 | B. | 乙酸、乙醇、四氯化碳 | ||
| C. | 苯、乙醇、四氯化碳 | D. | 苯、乙醇、乙酸 |
16.为了提纯下列物质(括号内为杂质 有关除杂试剂和分离方法的选择均正确的是( )
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 溴苯(溴) | 水 | 分液 |
| B | 乙醇(乙酸) | NaOH溶液 | 分液 |
| C | 甲烷(乙烯) | KMnO4酸性溶液 | 洗气 |
| D | 苯(苯酚) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
 →
→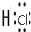 .
. 或
或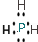 .
.