题目内容
14.下列对离子化合物的叙述不正确的是( )①离子化合物一定是含有离子键的化合物 ②离子化合物一定是由金属元素和非金属元素组成的③离子化合物熔点高,加热一定难分解 ④离子化合物中可能含有共价键,也可能不含共价键.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
分析 ①离子化合物是由阳离子和阴离子通过离子键结合构成的化合物;
②铵盐是由非金属元素形成的离子化合物;
③铵盐受热易分解;
④由不同元素组成的多原子分子里,一定存在极性共价键,可能含有非极性键.
解答 解:①离子化合物是由阳离子和阴离子通过离子键结合构成的化合物,所以离子化合物中一定是含有离子键的化合物,故正确.
②由非金属元素组成的化合物可能是离子化合物,如铵盐,是由非金属元素形成的离子化合物,故错误.
③铵盐属于离子化合物,铵盐受热易分解,则离子化合物加热不一定难分解,故错误.
④离子化合物中可能含有共价键,如NaOH;也可能不含共价键.如:NaCl,故正确.
故选:B
点评 本题考查化学键与化合物的类型,注意利用实例分析选项,把握特殊物质中的化学键及稀有气体中不含化学键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列对有关化学反应过程或实验现象的解释正确的是( )
| A. | 工业上用铝制容器盛装浓硫酸,说明常温下铝和浓硫酸不反应 | |
| B. | 在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si | |
| C. | 在空气中加热铝箔,发现内部的铝熔化但不滴落,说明铝不易与氧气反应 | |
| D. | 向淀粉碘化钾的溶液中加入氯水,溶液变为蓝色,说明Cl2的氧化性强于I2 |
9.电解含重水(D2O)的普通水.当电路中有4mo1电子通过时.测得两惰性电极上共产生36.5g气体.则在生成的气体中D和H的个数比为 ( )
| A. | 1:4 | B. | 1:5 | C. | 2:5 | D. | 1:7 |
19.下表是元素周期表的一部分,针对a~K十一种元素回答下列问题(请用具体化学式回答,否则不给分)
(1)这些元素中非金属性最强的单质是F2,最高价氧化物对应水化物酸性最强的是HClO4,最高价氧化物对应水化物碱性最强的是NaOH.
(2)表中K的氢化物的化学式为HCl,它的还原性比j的氢化物还原性弱(填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性强(填“强”或“弱”).
(3)e单质为N2,其结构式为N≡N.
(4)用电子式表示h与k构成化合物的形成过程
(5)写出i的氧化物与强碱溶液反应的离子方程式Al2O3+2OH-=2AlO2-+H2O
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热.将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应.下列说法正确的是ACD(填写选项).
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | a | c | d | e | f | g | |
| 3 | b | h | i | j | k |
(2)表中K的氢化物的化学式为HCl,它的还原性比j的氢化物还原性弱(填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性强(填“强”或“弱”).
(3)e单质为N2,其结构式为N≡N.
(4)用电子式表示h与k构成化合物的形成过程

(5)写出i的氧化物与强碱溶液反应的离子方程式Al2O3+2OH-=2AlO2-+H2O
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热.将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应.下列说法正确的是ACD(填写选项).
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡.
3.下列实验过程,无明显现象的是( )
| A. | 二氧化硫通入已酸化的硝酸钡溶液 | |
| B. | 二氧化氮通入氯化亚铁溶液中 | |
| C. | 氢氧化铝沉淀中滴加氨水 | |
| D. | 过量铜片与稀硝酸反应结束的溶液中加入稀硫酸 |
4.下列电离方程式错误的是( )
| A. | Ba(OH)2═Ba2++2OH- | B. | H2SO4═2H++SO42- | ||
| C. | NaHCO3═Na++H++CO3- | D. | NaCl═Na++Cl- |
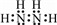 .
. ,N采用sp3杂化方式,粒子空间构型为V型.
,N采用sp3杂化方式,粒子空间构型为V型.