题目内容
 如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制480mL 1mol/L的稀硫酸.可供选用的仪器有:
如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制480mL 1mol/L的稀硫酸.可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平.
请回答下列问题:
(1)盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的

(2)配制稀硫酸时,还缺少的仪器有
(3)经计算,配制480mL 1 mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为
A.10mL B.50mL C.100mL D.200mL
(4)在烧杯中稀释浓硫酸的实验操作为
(5)对所配制的稀硫酸进行测定,发现其浓度大于1mol/L,配制过程中下列各项操作可能引起该误差的原因有
A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
B.定容时,俯视容量瓶刻度线进行定容
C.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作
D.转移溶液时,不慎有少量溶液洒到容量瓶外面
E.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处.
考点:化学试剂的分类,溶液的配制
专题:实验题
分析:(1)浓硫酸具有强烈的腐蚀性.
(2)根据配制溶液的实验操作过程选择所需的仪器.
(3)配制480mL稀硫酸,需要选用500mL容量瓶,根据溶液稀释过程中溶质的物质的量不变计算出需要浓硫酸的体积;根据浓硫酸的体积选择规格接近的量筒.
(4)浓硫酸稀释操作为将浓硫酸沿烧杯壁缓缓注入装有水的烧杯中,并用玻璃棒不断搅拌;
立即用抹布擦去,用大量水冲洗,涂上3%~5%NaHCO3的稀溶液.
((5)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
分析判断.
(2)根据配制溶液的实验操作过程选择所需的仪器.
(3)配制480mL稀硫酸,需要选用500mL容量瓶,根据溶液稀释过程中溶质的物质的量不变计算出需要浓硫酸的体积;根据浓硫酸的体积选择规格接近的量筒.
(4)浓硫酸稀释操作为将浓硫酸沿烧杯壁缓缓注入装有水的烧杯中,并用玻璃棒不断搅拌;
立即用抹布擦去,用大量水冲洗,涂上3%~5%NaHCO3的稀溶液.
((5)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
| n |
| V |
解答:
解:(1)浓硫酸具有强烈的腐蚀性,所以应标签上应印有腐蚀品标志.
故选:D.
(2)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.
由提供的仪器可知还需要仪器有:100mL容量瓶、玻璃棒.
(3)浓硫酸的物质的量浓度为:
=
mol/L=18.4mol/L,配制480mL 1mol?L-1的稀硫酸,实际上配制的是500mL 1mol?L-1的稀硫酸,需要浓硫酸的体积为:
≈0.0272L=27.2mL,需要选用50mL量筒,所以B正确.
故答案为:27.2;B;
(4)浓硫酸稀释操作为将浓硫酸沿烧杯壁缓缓注入装有水的烧杯中,并用玻璃棒不断搅拌;
少量浓硫酸不慎沾在手上,处理方法为:立即用抹布擦去,用大量水冲洗,涂上3%~5%NaHCO3的稀溶液.
故答案为:将浓硫酸沿烧杯壁缓缓注入装有水的烧杯中,并用玻璃棒不断搅拌;
立即用抹布擦去,用大量水冲洗,涂上3%~5%NaHCO3的稀溶液.
(5)A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸,量取浓硫酸的体积增大,所配溶液浓度偏高;
B.定容时,俯视容量瓶刻度线,导致所配溶液体积减小,所配溶液浓度偏高;
C.溶液有热胀冷缩的性质,浓硫酸稀释,放出大量的热,溶解后未恢复室温立即转移到容量瓶中定容,导致所配溶液体积减小,所配溶液浓度偏高;
D.转移溶液时,不慎有少量溶液洒到容量瓶外面,移入容量瓶中的溶质硫酸的物质的量减小,所配溶液浓度偏低;
E.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
F.摇匀后液面下降,一部分溶液留在瓶塞与瓶口之间,再加蒸馏水至刻度线,导致溶液体积偏大,所以溶液浓度偏低.
故选:ABC.
故选:D.
(2)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.
由提供的仪器可知还需要仪器有:100mL容量瓶、玻璃棒.
(3)浓硫酸的物质的量浓度为:
| 1000ρw |
| M |
| 1000×1.84×98% |
| 98 |
| 1mol/L×0.5L |
| 18.4mol/L |
故答案为:27.2;B;
(4)浓硫酸稀释操作为将浓硫酸沿烧杯壁缓缓注入装有水的烧杯中,并用玻璃棒不断搅拌;
少量浓硫酸不慎沾在手上,处理方法为:立即用抹布擦去,用大量水冲洗,涂上3%~5%NaHCO3的稀溶液.
故答案为:将浓硫酸沿烧杯壁缓缓注入装有水的烧杯中,并用玻璃棒不断搅拌;
立即用抹布擦去,用大量水冲洗,涂上3%~5%NaHCO3的稀溶液.
(5)A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸,量取浓硫酸的体积增大,所配溶液浓度偏高;
B.定容时,俯视容量瓶刻度线,导致所配溶液体积减小,所配溶液浓度偏高;
C.溶液有热胀冷缩的性质,浓硫酸稀释,放出大量的热,溶解后未恢复室温立即转移到容量瓶中定容,导致所配溶液体积减小,所配溶液浓度偏高;
D.转移溶液时,不慎有少量溶液洒到容量瓶外面,移入容量瓶中的溶质硫酸的物质的量减小,所配溶液浓度偏低;
E.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
F.摇匀后液面下降,一部分溶液留在瓶塞与瓶口之间,再加蒸馏水至刻度线,导致溶液体积偏大,所以溶液浓度偏低.
故选:ABC.
点评:本题考查了常见仪器的构造及其使用方法、配制一定物质的量浓度的方法,题目难度中等,注意掌握配制一定物质的量浓度的方法,明确常见仪器的构造及其使用方法.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
下列物质中,属于强电解质的是( )
| A、SO3 |
| B、C2H5OH |
| C、CH3COOH |
| D、CH3COONH4 |
我国稀土资源丰富,下列有关稀土元素
Sm与
Sm的说法不正确的是( )
| ||
| 62 |
| ||
| 62 |
| A、它们互为同位素 |
| B、它们是不同种核素 |
| C、它们的质量数相同 |
| D、它们的核外电指数相同 |
下列有关实验操作的说法正确的是( )
| A、用10mL量筒量取8.10mL稀盐酸 |
| B、用pH计测得某溶液的pH为2.2 |
| C、用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 |
| D、可用25mL酸式滴定管量取20.00mL KMnO4溶液 |
用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A:4HCl+O2
2Cl2+2H2O,可实现氯的循环利用.已知:Ⅰ.反应A中,4mol HCl被氧化,放出116kJ的热量.Ⅱ.拆开1mol o-o键需吸收498kJ的热量,拆开1mol Cl-Cl键需吸.收243kJ的热量.则断开1molH-O键与断开1molH-Cl键所需能量相差为( )
| ||
| 400℃ |
| A、16kJ | B、24kJ |
| C、32kJ | D、48kJ |
某溶液中可能含有I-、NH4+、Cu2+、SO32-,向该无色溶液中加入少量溴水,溶液仍呈无色,则下列关于该溶液组成的判断不正确的是( )
| A、肯定不含I- |
| B、肯定不含Cu2+ |
| C、肯定含有SO32- |
| D、可能含有I- |
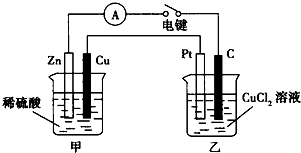 某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流表的指针发生了偏转.
某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流表的指针发生了偏转.