题目内容
16. 下列各项中的物质,能满足如图中阴影部分关系的是( )
下列各项中的物质,能满足如图中阴影部分关系的是( )| ① | ② | ③ | ④ | |
| A | NaCl | K2SO4 | KCl | (NH4)2SO4 |
| B | NaCl | K2SO4 | KCl | NH4Cl |
| C | Na2SO4 | K2SO4 | KCl | NH4Cl |
| D | Na2SO4 | K2SO4 | KCl | (NH4)2SO4 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据盐电离出的阴阳离子的种类分类即可,例如阳离子为钠离子的盐统称为钠盐,阴离子为硫酸根离子的盐统称为硫酸盐.
解答 解:A.①NaCl属于盐酸盐,不是硫酸盐,④(NH4)2SO4属于硫酸盐,不是盐酸盐,故A错误;
B.①NaCl属于盐酸盐,不是硫酸盐,故B错误;
C.各项均符合,故C正确;
D.④(NH4)2SO4属于硫酸盐,不是盐酸盐,故D错误;
故选C.
点评 本题考查了盐的分类,把握分类依据分析即可解答,题目难度不大.

练习册系列答案
相关题目
7.在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质.下列实验现象和结论一定正确的是( )
| A. | 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在 | |
| B. | 向氯水中滴加石蕊试液,溶液先变红后褪色,说明溶液中有盐酸和次氯酸 | |
| C. | 加入盐酸酸化,再加入硝酸银溶液产生白色沉淀,说明氯水中有Cl-存在 | |
| D. | 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在 |
1.在标准状况下,等质量的CH4和CO2比较,下列说法中正确的是( )
| A. | 密度比4:11 | B. | 分子数之比为4:11 | ||
| C. | 体积比4:11 | D. | 物质的量之比为4:11 |
8.下列离子方程式书写正确的是( )
| A. | 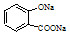 溶液通入少量CO2: 溶液通入少量CO2: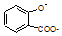 +CO2+H2O═ +CO2+H2O═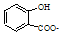 +HCO3- +HCO3- | |
| B. | 水电离产生的c(H+)=10-12mol•L-1的溶液中:Na+、Fe2+、SO42-、NO3-可能会大量共存 | |
| C. | 少量SO2通入NaClO溶液中:SO2+ClO-+OH-=SO42-+Cl-+H+ | |
| D. | 5.6 g Fe与200 mL 2.0 mol/L HNO3溶液:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O |
5.下列有关实验操作设计、现象记录、结论解释都正确的是( )
| 选项 | 实验操作设计 | 现象记录 | 结论解释 |
| A | 将少量浓硝酸逐滴加入Cu和稀硫酸的混合物中 | 产生红棕色气体 | 硝酸被还原为NO2 |
| B | 用坩埚钳夹住铝箔在酒精灯上加热 | 铝箔熔化但并不滴落 | 熔点:Al2O3>Al |
| C | 向某氯化亚铁溶液中加入 Na2O2粉末 | 出现红褐色沉淀 | 加入Na2O2粉末前,原氯化亚铁溶液已经变质 |
| D | 向AlCl3溶液中逐滴加入NaOH溶液至过量 | 产生大量的白色沉淀 | Al(OH)3难溶于水 |
| A. | A | B. | B | C. | C | D. | D |
14.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | c(H+)/c(OH?)=1的无色溶液中:Fe3+、NH4+、Cl?、SO42? | |
| B. | 使甲基橙呈黄色的溶液中:Na+、ClO?、SO42?、I? | |
| C. | 0.1 mol•L-1NaAlO2溶液:H+、Na+、Cl-、SO42- | |
| D. | pH=12的溶液:K+、Na+、CH3COO-、Br- |

 .
. .
.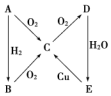 根据如图所示转化关系,判断A、B、C、D各是什么物质,写出有关的化学方程式:
根据如图所示转化关系,判断A、B、C、D各是什么物质,写出有关的化学方程式: