题目内容
用H2还原xgCuO,当大部分固体变红时停止加热,冷却后得残留固体yg,共用掉z g H2,此时生成水的质量为( )
A、
| ||
B、
| ||
| C、9 z g | ||
D、
|
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:H2+CuO
Cu+H2O,防止生成的铜被氧化,要继续通入氢气直至冷却,可知用去z g氢气并未全部参加还原氧化铜的反应,所以不能用氢气质量计算生成水的质量,反应前后固体质量差为氧化铜在反应中失去氧元素的质量,失去的氧元素与氢化合成水,由氧元素质量可计算生成水的质量.
| ||
解答:
解:发生反应:H2+CuO
Cu+H2O,防止生成的铜被氧化,要继续通入氢气直至冷却,可知用去z g氢气并未全部参加还原氧化铜的反应,所以不能用氢气质量计算生成水的质量,反应前后固体质量差为氧化铜在反应中失去氧元素的质量,故反应中氧化铜失去O元素的质量=xg-yg=(x-y)g,
含(x-y)g氧元素的水的质量=(x-y)g÷
=
g,
故选B.
| ||
含(x-y)g氧元素的水的质量=(x-y)g÷
| 16 |
| 18 |
| 9(x-y) |
| 8 |
故选B.
点评:本题考查化学方程式的有关计算,明确固体质量变化是解题关键,侧重考查学生的分析思维能力,C选项为易错点,学生容易忽略“为防止生成的铜被氧化,要继续通入氢气直至冷却”,难度不大.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
现有常温时pH=1的硫酸溶液10mL,下列操作能使溶液的pH变成2的是( )
| A、加热 |
| B、加入100 mL的水进行稀释 |
| C、加入90mL 0.1 mol?L-1的NaOH溶液 |
| D、加入10 mL 0.01 mol?L-1的盐酸 |
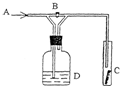 如图是一种试验氯气化学性质的实验装置,图中B为开关. 如先打开B,再让一种含氯气的气体从A处通入,C中干燥红色布条颜色褪色;当关闭B时,C处红色布条颜色无变化.则D瓶中盛有的溶液是( )
如图是一种试验氯气化学性质的实验装置,图中B为开关. 如先打开B,再让一种含氯气的气体从A处通入,C中干燥红色布条颜色褪色;当关闭B时,C处红色布条颜色无变化.则D瓶中盛有的溶液是( )①浓H2SO4②饱和NaCl溶液 ③浓NaOH溶液 ④饱和碳酸氢钠.
| A、①②③ | B、②③④ |
| C、①②④ | D、①③④ |
酚醛树脂可用苯酚和甲醛反应制得.实验室制备酚醛树脂时,在酸性条件下,苯酚过量制得酚醛树脂若不易取出,则可趁热时加入一些乙醇来取出酚醛树脂;在碱性条件下,苯酚过量时,若酚醛树脂不易取出时,用加热或加溶剂的方法都很难将酚醛树脂取出.在上述两种情况下,下列有关叙述正确的是( )
| A、酸性条件制得的是体型结构酚醛树脂,碱性条件制得的是线型结构酚醛树脂 |
| B、酸性条件制得的是线型结构酚醛树脂,碱性条件制得的是网状结构酚醛树脂 |
| C、两种条件下制得的都是线型结构的酚醛树脂 |
| D、两种条件下制得的都是网状结构酚醛树脂 |
有①、②、③三瓶体积相等,浓度都是1mol/L的H2SO4溶液,将①加热蒸发至体积减小一半,在②中加入CH3COONa固体(加入后溶液仍呈酸性),③不作改变,然后以酚酞作指示剂,用NaOH溶液滴定上述三种溶液,消耗的NaOH溶液的体积是( )
| A、①=③>② |
| B、③>②>① |
| C、①=②=③ |
| D、①<②=③ |
下列说法不正确的是( )
| A、Mg的金属性比Al强 |
| B、H2S的热稳定性比H2O强 |
| C、Na的原子半径比N原子大 |
| D、HClO4的酸性比H3PO4强 |
