题目内容
5.质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是SO2,在相同温度和相同压强条件下,体积最大的是H2.分析 根据N=nNA=$\frac{m}{M}$×NA可知气体的摩尔质量越大,含有的分子数越小;根据V=$\frac{m}{M}$×Vm可知,摩尔质量越小,气体体积越大,据此进行解答.
解答 解:质量相同的H2、NH3、SO2、O3四种气体中,N=nNA=$\frac{m}{M}$×NA可知,质量相同时气体分子数与摩尔质量成反比,摩尔质量越大,含有的分子数越小,所以含有分子数最少的是摩尔质量最大的为SO2;
由V=$\frac{m}{M}$×Vm可知,质量相同时,气体体积与摩尔质量成反比,体积最大的是气体摩尔质量最小的,则体积增大的为H2,
故答案为:SO2; H2.
点评 本题考查了物质的量的简单计算,题目难度不大,注意掌握物质的量与阿伏伽德罗常数、摩尔质量、气体摩尔体积之间的关系,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
16.下列物质中不能由化合反应生成的物质是( )
| A. | FeCl3 | B. | H2SO4 | C. | NaHCO3 | D. | Fe2S3 |
13.下列关于热化学反应的描述中正确的是( )
| A. | CO(g)的燃烧热是283.0 kJ•mol-1,则反应2CO2(g)=2CO(g)+O2(g)的△H=2×283.0 kJ•mol-1 | |
| B. | 1mol甲烷完全燃烧生成二氧化碳和水蒸汽所放出的热量是甲烷的燃烧热 | |
| C. | 已知由石墨制备金刚石为吸热反应,则金刚石比石墨稳定 | |
| D. | HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ•mol-1 |
20.下列情况下,气体分子数相同的是( )
| A. | 标准状况下,71gCl2和22.4LHCl | B. | 相同质量的氢气和氮气 | ||
| C. | 在0℃时,1体积的O2和1体积的HCl | D. | 相同体积的CO2和 H2O |
10.将乙醇滴入热的浓硫酸中,发生反应:C2H5OH+6H2SO4=6SO2↑+2CO2↑+9H2O,浓硫酸没有体现的性质是( )
| A. | 氧化性 | B. | 脱水性 | C. | 酸性 | D. | 吸水性 |
17.稀氨水中存在电离平衡:NH3•H2O?NH4++OH-,若要使平衡正向移动,同时使c(OH-)减小,应加入的物质或采取的措施是( )
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤通入HCl ⑥加入少量MgSO4固体.
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤通入HCl ⑥加入少量MgSO4固体.
| A. | ①②⑤ | B. | ①③⑥ | C. | ②④⑤ | D. | ②④⑤⑥ |
14.将下列各组物质按酸、碱、盐分类顺次排列,其中正确的是( )
| A. | 硫酸 纯碱 孔雀石[Cu2(OH)2CO3] | B. | 硝酸 烧碱 硫酸钡 | ||
| C. | 醋酸 乙醇 碳酸钙 | D. | 盐酸 熟石灰 苛性钠 |
15.己烯雌酚是一种激素类药物,其结构简式如图所示,下列有关叙述中错误的是( )
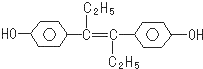

| A. | 己烯雌酚分子中碳原子的杂化轨道方式有sp2和sp3两种 | |
| B. | 己烯雌酚分子中所有的原子都可能在一个平面内 | |
| C. | 1mol己烯雌酚分子与溴水完全反应时,最多可消耗5molBr2 | |
| D. | 1mol己烯雌酚分子与氢气在一定条件下完全反应时,最多可消耗7molH2 |