题目内容
 碳酸钙可以降低胃酸的浓度而被用作胃药的抗酸剂.某中学研究性学习小组为测定一胃药中碳酸钙的含量,设计了如下的实验操作:
碳酸钙可以降低胃酸的浓度而被用作胃药的抗酸剂.某中学研究性学习小组为测定一胃药中碳酸钙的含量,设计了如下的实验操作:①配制0.1 mol?L-1的HCl溶液和0.1 mol?L-1的NaOH溶液各100mL;
②取一粒(药片质量均相同)0.2g的此药片,磨碎后放入烧杯中并加入20.0mL蒸馏水;
③以酚酞为指示剂,用0.1 mol?L-1的NaOH溶液滴定,用去V mL达到滴定终点;
④向烧杯中加入25mL 0.1 mol?L-1的HCl溶液.
(1)请写出正确的实验操作顺序(用序号表示):
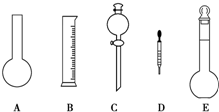
(2)在如图所示的仪器中配制0.1 mol?L-1的HCl溶液和0.1 mol?L-1的NaOH溶液肯定不需要的是(填序号)
(3)配制上述溶液应选用的容量瓶规格是
(4)写出步骤④中发生的有关反应的离子方程式:
(5)在进行步骤③时,判断到达滴定终点时的标志是
(6)每粒该胃药中含碳酸钙的质量是
考点:中和滴定,配制一定物质的量浓度的溶液
专题:实验题
分析:(1)用中和滴定法胃药中碳酸钙的含量,先把药片磨碎溶于水,配制0.1 mol?L-1的HCl溶液和0.1 mol?L-1的NaOH溶液,加过量的盐酸溶解碳酸钙,再用氢氧化钠滴定剩余的盐酸;
(2)配制溶液的主要操作为:称量或量取、在烧杯中溶解、转移到容量瓶、定容;
(3)根据配制的溶液体积选择容量瓶;
(4)步骤④中为盐酸与碳酸钙反应;
(5)以酚酞作指示剂,用氢氧化钠滴定盐酸,溶液由无色变为浅红色;
(6)根据氢氧化钠的量求出盐酸的量,用总的盐酸的物质的量减去与氢氧化钠反应的盐酸的量即是与碳酸钙反应的盐酸的量,根据方程式计算出碳酸钙的物质的量,再求质量.
(2)配制溶液的主要操作为:称量或量取、在烧杯中溶解、转移到容量瓶、定容;
(3)根据配制的溶液体积选择容量瓶;
(4)步骤④中为盐酸与碳酸钙反应;
(5)以酚酞作指示剂,用氢氧化钠滴定盐酸,溶液由无色变为浅红色;
(6)根据氢氧化钠的量求出盐酸的量,用总的盐酸的物质的量减去与氢氧化钠反应的盐酸的量即是与碳酸钙反应的盐酸的量,根据方程式计算出碳酸钙的物质的量,再求质量.
解答:
解:(1)用中和滴定法胃药中碳酸钙的含量,先把药片磨碎溶于水,配制0.1 mol?L-1的HCl溶液和0.1 mol?L-1的NaOH溶液,加过量的盐酸溶解碳酸钙,再用氢氧化钠滴定剩余的盐酸,则实验操作顺序为②①④③;
(2)配制溶液的主要操作为:称量或量取用到天平或量筒、在烧杯中溶解用到烧饼和玻璃棒、转移到容量瓶用到容量瓶和玻璃棒、定容用到胶头滴管,所以没有用到的仪器是烧瓶和分液漏斗,即AC;除了图中所给的仪器还需要烧杯和玻璃棒;
故答案为:AC;烧杯、玻璃棒;
(3)要配制100ml盐酸和氢氧化钠溶液,所以选用100ml的容量瓶;
故答案为:100;
(4)步骤④中为盐酸与碳酸钙反应生成氯化钙、二氧化碳和水,其反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O;
故答案为:CaCO3+2H+═Ca2++CO2↑+H2O;
(5)以酚酞作指示剂,用氢氧化钠滴定盐酸,溶液由无色变为浅红色,则滴入最后一滴NaOH溶液时,使溶液由无色变为浅红色,且半分钟内不褪色即是滴定终点;
故答案为:滴入最后一滴NaOH溶液时,使溶液由无色变为浅红色,且半分钟内不褪色;
(6)与氢氧化钠反应的盐酸为n(HCl)=n(NaOH)=0.1 mol?L-1×10-3VL=10-4Vmol;
与碳酸钙反应的盐酸为n′(HCl)=0.1 mol?L-1×0.025L-10-4Vmol=(0.0025-10-4V)mol,
已知碳酸钙与盐酸的反应为:CaCO3+2H+═Ca2++CO2↑+H2O,则n(CaCO3)=
×(0.0025-10-4V)mol,
则每粒该胃药中含碳酸钙的质量是
×(0.0025-10-4V)mol×100g/mol=(0.125-0.005V)g;
故答案为:(0.125-0.005V)g.
(2)配制溶液的主要操作为:称量或量取用到天平或量筒、在烧杯中溶解用到烧饼和玻璃棒、转移到容量瓶用到容量瓶和玻璃棒、定容用到胶头滴管,所以没有用到的仪器是烧瓶和分液漏斗,即AC;除了图中所给的仪器还需要烧杯和玻璃棒;
故答案为:AC;烧杯、玻璃棒;
(3)要配制100ml盐酸和氢氧化钠溶液,所以选用100ml的容量瓶;
故答案为:100;
(4)步骤④中为盐酸与碳酸钙反应生成氯化钙、二氧化碳和水,其反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O;
故答案为:CaCO3+2H+═Ca2++CO2↑+H2O;
(5)以酚酞作指示剂,用氢氧化钠滴定盐酸,溶液由无色变为浅红色,则滴入最后一滴NaOH溶液时,使溶液由无色变为浅红色,且半分钟内不褪色即是滴定终点;
故答案为:滴入最后一滴NaOH溶液时,使溶液由无色变为浅红色,且半分钟内不褪色;
(6)与氢氧化钠反应的盐酸为n(HCl)=n(NaOH)=0.1 mol?L-1×10-3VL=10-4Vmol;
与碳酸钙反应的盐酸为n′(HCl)=0.1 mol?L-1×0.025L-10-4Vmol=(0.0025-10-4V)mol,
已知碳酸钙与盐酸的反应为:CaCO3+2H+═Ca2++CO2↑+H2O,则n(CaCO3)=
| 1 |
| 2 |
则每粒该胃药中含碳酸钙的质量是
| 1 |
| 2 |
故答案为:(0.125-0.005V)g.
点评:本题考查溶液的配制、中和滴定、物质含量的测定,题目难度中等,侧重于学生的分析能力和实验能力的考查,注意把握实验原理、步骤和操作注意事项等.

练习册系列答案
相关题目
胶体区别于其它分散系的实质是( )
| A、胶体粒子直径在1nm-100nm之间 |
| B、胶体可发生丁达尔效应 |
| C、胶体粒子不能透过半透膜 |
| D、胶体粒子能够发生布朗运动 |

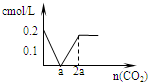
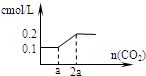
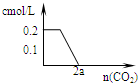
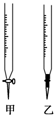 某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步: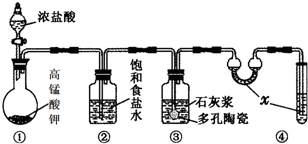 实验室常用以下几种方法制取氯气
实验室常用以下几种方法制取氯气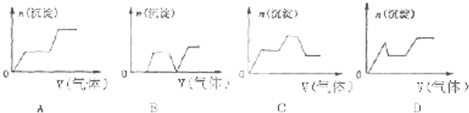
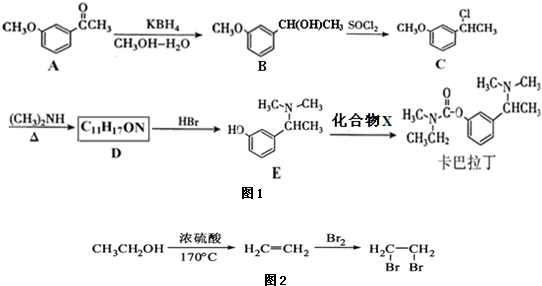
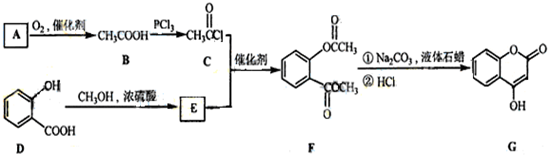
 )和丙酮(
)和丙酮( )制备化合物
)制备化合物 的合成路线流程图(无机试剂任选).合成路线流程图如图2:
的合成路线流程图(无机试剂任选).合成路线流程图如图2: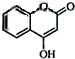 是一种医药中间体,常用来制备抗凝血药,可通过如图路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过如图路线合成: