题目内容
3.铜仁一中高一年级某化学兴趣小组欲除去粗盐中的可溶性杂质CaCl2、MgCl2、Na2SO4,他们先将粗盐溶于水,然后依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液,过滤后加过量的稀盐酸,最后经过蒸发操作,就得到了纯净的NaCl固体.分析 选碳酸钠除去氯化钙、选NaOH除去氯化镁,选氯化钡除去硫酸钠,且碳酸钠在氯化钡之后,可除去过量的钡离子,过滤后加盐酸除去过量碳酸钠,蒸发可得到NaCl.
解答 解:除去粗盐中的可溶性杂质CaCl2、MgCl2、Na2SO4,他们先将粗盐溶于水,然后依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液,过滤后加过量的稀盐酸,最后经过蒸发操作,就得到了纯净的NaCl固体,
故答案为:BaCl2;Na2CO3;稀盐酸;蒸发.
点评 本题考查粗盐提纯,为高频考点,把握除杂试剂的选择、先后顺序及除杂原则为解答的关键,侧重分析与实验能力的考查,注意碳酸钠在氯化钡之后,题目难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
12.已知甲烷和汽油(可用C8H18表示)的燃烧的热化学方程式:
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1;
C8H18(l)+12.5O2(g)═8CO2(g)+9H2O(l)△H=-5472kJ•mol-1;
某学校食堂拟选用天然气作为供热燃料,下列选择依据不正确的是( )
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1;
C8H18(l)+12.5O2(g)═8CO2(g)+9H2O(l)△H=-5472kJ•mol-1;
某学校食堂拟选用天然气作为供热燃料,下列选择依据不正确的是( )
| A. | 等质量的汽油和甲烷燃烧,甲烷产生的热量比汽油多,因此甲烷更高效 | |
| B. | 产生相同热量所生成的二氧化碳,汽油比甲烷多,因此甲烷更低效 | |
| C. | 甲烷含碳量低,燃烧更充分,不易积炭,不易产生CO,因此更环保 | |
| D. | 等物质的量的汽油和甲烷燃烧,汽油产生的热量比甲烷多,因此更环保 |
13.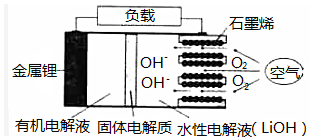 新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )
新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )
 新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )
新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )| A. | 放电时,负极反应式:Li-e-+OH-═LiOH | |
| B. | 放电时,当外电路中有1mole-转移时,水性电解液离子总数增加NA | |
| C. | 应用该电池电镀铜,阴极质量增加64g,理沦上将消耗11.2LO2 | |
| D. | 若把水性电解液换成固体氧化物电解质,则易引起正极材料碳孔堵塞 |
11.有关化学与生活,环境,食品安全,材料等说法中正确的是( )
| A. | 大气中大量的NO、NO2等酸性氧化物均是形成酸雨(PH>5.6)的主要原因 | |
| B. | 合成纤维,光导纤维,硝酸纤维均为有机高分子物质,用途广泛 | |
| C. | 二氧化硫和氯水均具有漂白性,可将两者混合使用增强漂白效果 | |
| D. | 地沟油,潲水油在餐饮企业中不能随意使用,但却可以用于制肥皂,变废为宝 |
8.下列关于常温下电解质溶液的说法正确的是( )
| A. | 0.1mol•L-1的HF溶液加水稀释过程中,HF的电离平衡常数逐渐增大 | |
| B. | pH=12的NaOH溶液与pH=2的醋酸溶液等体积混合后,溶液呈中性 | |
| C. | pH=5的NaHSO3溶液中水电离出的H+浓度小于10-71mol•L-1 | |
| D. | 向Na2CO3,Na2SO4的混合溶液中逐滴加入BaCl2溶液,一定先生成BaSO4 |
15.下列说法正确的是( )
| A. | 含H+的溶液显酸性 | |
| B. | 加热蒸馏水,Kw变大,pH变小 | |
| C. | 常温下,0.01mol•L-1的Ba(OH)2溶液pH为12 | |
| D. | 醋酸溶液加水稀释,所有离子的浓度都减小 |
13.下列有关物质的性质或应用的说法正确的是( )
| A. | 用核磁共振氢谱鉴别1-丙醇和2-丙醇 | |
| B. | 在甲苯中加入少量酸性高锰酸钾溶液,振荡后褪色 | |
| C. | 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 | |
| D. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
 碱式碳酸镁和无水氯化镁具有广泛的用途.用白云石(CaCO3•MgCO3)为主要原料生产碱式碳酸镁和无水氯化镁的流程如图:回答问题:
碱式碳酸镁和无水氯化镁具有广泛的用途.用白云石(CaCO3•MgCO3)为主要原料生产碱式碳酸镁和无水氯化镁的流程如图:回答问题: