题目内容
20.下列有机物属于烷烃的是( )| A. | C2H4 | B. | C4H6 | C. | C3H8 | D. | C6H6 |
分析 烷烃分子结构中碳原子为饱和碳原子,烷烃同系物符合通式CnH2n+2,据此分析选项;
解答 解:烷烃分子结构中碳原子为饱和碳原子,需要符合通式CnH2n+2,
A.C2H4不符合通式CnH2n+2,结构不同,故A错误;
B.C4H6 不符合通式CnH2n+2,结构不同,故B错误;
C.C3H8符合通式CnH2n+2,结构相似,组成相差CH2,是烷烃同系物,故C正确;
D.C6H6不符合通式CnH2n+2,结构不同,故D错误;
故选C.
点评 本题考查了同系物概念的内涵和外延,注意结构的不同,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
10.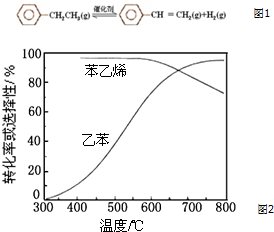 乙苯催化脱氢制苯乙烯反应如图1:
乙苯催化脱氢制苯乙烯反应如图1:
(1)已知:
反应的△H=+124kJ•mol-1,X=412kJ•mol-1.
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应.已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=$\frac{α{\;}^{2}}{(1-α{\;}^{2})}p$(用α等符号表示),在平衡体系中充入氖气反应速率将减小(填“增大”“减小”“不变”).
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1:9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应.在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如图1:
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动.
②控制反应温度为600℃的理由是600℃时乙苯的转化率与苯乙烯的选择性均较高,温度过低,反应速率较慢,转化率较低,温度过高,选择性下降,高温下可能失催化剂失去活性,且消耗能量较大.
(4)某研究机构用CO2代替水蒸气开发了绿色化学合成工艺--乙苯-二氧化碳耦合催化脱氢制苯乙烯.保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2═CO+H2O,CO2+C═2CO.新工艺的特点有①②③④(填编号).
①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利于CO2资源利用
(5)产物中另一种物质常用做燃料电池的材料,若电解质为熔融碳酸盐,其负极电极反应式为H2-2e-+CO32-=H2O+CO2↑.
 乙苯催化脱氢制苯乙烯反应如图1:
乙苯催化脱氢制苯乙烯反应如图1:(1)已知:
| 化学键 | C-H | C-C | C═C | H-H |
| 键能/kJ•mol-1 | X | 348 | 612 | 436 |
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应.已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=$\frac{α{\;}^{2}}{(1-α{\;}^{2})}p$(用α等符号表示),在平衡体系中充入氖气反应速率将减小(填“增大”“减小”“不变”).
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1:9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应.在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如图1:
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动.
②控制反应温度为600℃的理由是600℃时乙苯的转化率与苯乙烯的选择性均较高,温度过低,反应速率较慢,转化率较低,温度过高,选择性下降,高温下可能失催化剂失去活性,且消耗能量较大.
(4)某研究机构用CO2代替水蒸气开发了绿色化学合成工艺--乙苯-二氧化碳耦合催化脱氢制苯乙烯.保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2═CO+H2O,CO2+C═2CO.新工艺的特点有①②③④(填编号).
①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利于CO2资源利用
(5)产物中另一种物质常用做燃料电池的材料,若电解质为熔融碳酸盐,其负极电极反应式为H2-2e-+CO32-=H2O+CO2↑.
11.标况下,2.2gCH4和C2H4组成的混合气体所占的体积为2.24L,则该混合气中CH4和C2H4的比值是( )
| A. | 摩尔比1:1 | B. | 摩尔比1:2 | C. | 质量比1:1 | D. | 质量比7:4 |
8.下列化合物,依次属于氧化物、碱、盐的一组是( )
| A. | Na2CO3、KOH、CaO | B. | CO、NaOH、KCl | ||
| C. | H2O、H2SO4、NaCl | D. | CuO、Cu2(OH)2CO3、CaCO3 |
15.最近医学界通过用放射性14C标记C60,发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病(AIDS).下列有关14C的叙述正确的是( )
| A. | 14C与C60中普通碳原子的化学性质不同 | |
| B. | 14C与14N含的中子数相同 | |
| C. | 14C是C60的同素异形体 | |
| D. | 14C与12C互为同位素 |
5.有机物Ⅰ和Ⅱ的结构式如下,下列说法中正确的是( )
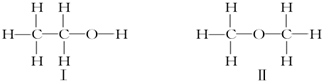
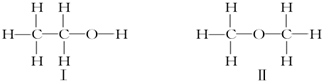
| A. | Ⅰ和Ⅱ是同分异构体 | B. | Ⅰ和Ⅱ物理性质完全相同 | ||
| C. | Ⅰ和Ⅱ化学性质相同 | D. | Ⅰ和Ⅱ的分子式不相同 |
12.用铝片和稀硫酸反应制取氢气时,下列做法能加快化学反应速率的是(
| A. | 用98%的浓硫酸替代稀硫酸 | B. | 降低温度 | ||
| C. | 用铝粉代替铝片 | D. | 加入Na2SO4溶液 |
9.下列变化中,不属于化学变化的是( )
| A. | 石墨变成金刚石 | B. | 胆矾(CuSO4•5H2O)失去结晶水 | ||
| C. | 氯气变成液氯 | D. | 白磷转化为红磷 |
10.“纳米材料”是指粒子直径在几纳米到几十纳米的材料.若将“纳米材料”分散到液体分散剂中,所得混合物具有的性质是( )
| A. | 能全部透过半透膜 | |
| B. | 能产生丁达尔效应 | |
| C. | 所得液体一定能导电 | |
| D. | 所得混合物不稳定,静置后容易产生沉淀 |