题目内容
现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p3;④1s22s22p5。则下列有关比较中正确的是 ( )
| A.第一电离能:④>③>②>① | B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① | D.最高正化合价:④>③=②>① |
A
解析试题分析:根据电子排布式可知①为S,②为P,③为N,④为F,A、第一电离能的顺序为F>N>P>S,正确;B、原子半径:P>S>N>F,错误;C、电负性:S>P,错误;D、F无正化合价,错误。
考点:本题考查电子排布与元素的性质。

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
下列关于 、
、 、
、 的说法正确的是
的说法正确的是
| A.它们的物理性质相似 | B.它们是碳元素的三种核素 |
| C.它们是碳元素的三种单质 | D.它们是碳元素的同素异形体 |
X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
| | X | Y | Z | M | R | Q |
| 原子半径/nm | | | 0.186 | 0.074 | 0.099 | 0.143 |
| 主要化合价 | | -4,+4 | | -2 | -1,+7 | +3 |
| 其它 | 阳离子核 外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 | | | |
下列说法正确的是
A.X与M形成的化合物中含有离子键
B.Z、M、Q三种元素的简单离子的半径:M>Z>Q
C.Y与R形成的化合物中R呈正价,说明Y的非金属性比R强
D.在元素周期表中,Q位于金属与非金属的交界处,可以作半导体材料
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为11;Y、
Z在同一周期;Z原子最外层电子数是X原子内层电子数的2倍,也是Y原子最外层电子数的2倍。下列说法中,正确的是( )
| A.离子半径:Y>X | B.气态氢化物的稳定性:Z>X |
| C.Y的氧化物中含有离子键 | D.Z的氧化物对应的水化物是弱碱 |
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g ? L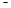 1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是( )
1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是( )
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由Y、Z、M三种元素形成的化合物一定只有共价键 |
下列事实与氢键有关的是
| A.HF、HCl、HBr、HI的热稳定性依次减弱 |
| B.水加热到很高的温度都难以分解 |
| C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 |
| D.水结成冰体积膨胀 |
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且将a、b相连浸入稀硫酸中时,a溶解而b表面有气泡产生;c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是( )
| A.a、b、e、d、c | B.e、d、a、b、c |
| C.b、a、e、d、c | D.a、b、d、c、e |
四种短周期元素在周期表中的相对位置如右表所示,下列说法错误的是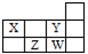
| A.X和Y元素的原子最外层电子数之和等于Z元素的原子最外层电子数的2倍 |
| B.Y元素的非金属性强于W元素的,其最高价氧化物水化物的酸性也强于W的 |
| C.X最简单氢化物溶于水呈碱性,Z最简单氢化物溶于水呈酸性 |
| D.W元素形成的单质可以从Z元素氢化物的水溶液中置换出Z单质 |
根据中学化学教材所附元素周期表判断,下列叙述不正确的是( )
| A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等 |
| B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等 |
| C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等 |
| D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等 |