题目内容
实验室常用盐酸的质量分数为36.5%,密度为1.20g/㎝3。
⑴此浓盐酸的物质的量浓度是多少?(列式计算)
⑵配制100mL3.00mol/L的盐酸,需以上浓盐酸多少mL ?(列式计算)
⑶用浓盐酸配制该稀盐酸需要以下哪些步骤(按操作顺序填写序号): 。
①计算 ②装瓶③用50 mL量筒量取一定体积的浓盐酸④洗涤⑤移液⑥稀释⑦定容⑧摇匀
(1)12.0mol/L(2)25ml(3)①③⑥⑤④⑦⑧②.
解析试题分析:(1)设盐酸溶液的体积为1L,则溶液的质量为1000ml×1.20g/ml,溶质的物质的量为 =12.0mol,C(HCl)=12.0mol/L,此浓盐酸的物质的量浓度是12.0mol/L.
=12.0mol,C(HCl)=12.0mol/L,此浓盐酸的物质的量浓度是12.0mol/L.
(2)根据溶液稀释前后溶质的物质的量不变,则有C(浓)?V(浓)=C(稀)?V(稀),
即12.0mol/L×V(浓)=0.1L×3.00mol/L,则需浓盐酸V(浓)= =0.025L=25ml
=0.025L=25ml
答:配制100mL3.00mol/L的盐酸,需以上浓盐酸25mL.
(3)配制一定物质的量浓度的溶液需要量取、溶解、移液、洗涤、定容、摇匀等操作,其先后顺序为
①③⑥⑤④⑦⑧②,故答案为:①③⑥⑤④⑦⑧②.
考点:配置一定物质的量浓度的溶液及相关计算

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案下列对合金描述不正确的是
| A.合金最多只能含有两种元素 |
| B.多数合金的硬度较大 |
| C.多数合金的熔点比成分金属低 |
| D.合金的性能跟合金元素的种类有关 |
化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是
①加快化石燃料的开采与使用;②研发易降解的生物农药;③应用高效洁净的能源转化技术;
④田间焚烧秸秆;⑤推广使用节能环保材料。
| A.①③⑤ | B.②③⑤ | C.①②④ | D.②④⑤ |
下列环境问题主要与SO2有关的是
| A.臭氧空洞 | B.酸雨 | C.光化学烟雾 | D.温室效应 |
2013年下半年,武汉雾霾天气特别多,空气污染严重。湖北省决定在“十二五”期间,将大力实施“清水蓝天”工程。不利于“清水蓝天”工程实施的是 ( )
| A.加强城市生活污水脱氮除磷处理,遏制水体富营养化 |
| B.为防止电池中的重金属污染,废旧电池应作深埋处理 |
| C.积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用 |
| D.大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染 |
(10分)某同学帮助水质检测站配制800mL 1 mol·L-1NaOH溶液备用。
(1)该同学应选择的玻璃仪器除了烧杯、量筒、玻璃棒、胶头滴管外,还有 。
(2)其操作步骤如下图所示,则如图操作应在下图中的 (填选项字母)之间。
| A.②与③ | B.①与② | C.④与⑤ | D.③与④ |

(3)该同学应用托盘天平称取NaOH固体 g,用质量为33.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在下图中选出能正确表示游码位置的选项 (填选项字母)。

(4)下列操作对所配溶液浓度大小有何影响 (填“偏大”、“偏小”或“无影响”)。
①定容时,仰视读数,浓度会 ;
②转移溶液过程中,未洗涤玻璃棒和烧杯,浓度会 ;
③容量瓶未干燥,浓度会 ;
④定容摇匀后发现溶液凹面低于刻度线,继续加水至刻度线,浓度会 。
(5)配制溶液的实际操作过程中,动作要快,否则由于 ,会使配制的NaOH溶液的浓度比1 mol·L-1______(填“大”或“小”)。
(10分)某同学帮助水质检测站配制480 mL 0.5 mol·L-1 NaOH溶液以备使用。
(1)该同学应选择________mL的容量瓶。
(2)其操作步骤如下图所示,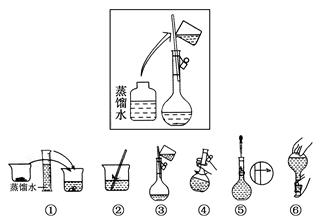
则如图操作应在下图中的________(填选项字母)之间。
A.②与③ B.①与② C.④与⑤
(3)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小________(填字母),并在下图中选出能正确表示游码位置的选项________(填字母)。
附表 砝码规格
| | a | b | c | d | e |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
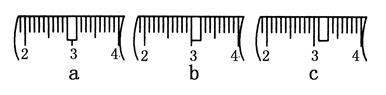
(4)下列操作对所配溶液的浓度大小有何影响?
①转移完溶液后未洗涤玻璃棒和烧杯,浓度会________(填“偏大”、“偏小”或“无影响”,下同)
②容量瓶中原来有少量蒸馏水,浓度会________。