题目内容
120℃和101kPa时,甲烷、乙烯和乙炔组成的混合烃32mL,与过量氧气混合并完全燃烧,恢复到原来的温度和压强,气体总体积缩小了8mL,原混合烃中乙炔的体积分数为( )
| A、12.5% | B、25% |
| C、50% | D、75% |
考点:有关混合物反应的计算
专题:计算题
分析:发生反应分别为:CH4+2O2
CO2+2H2O?,C2H4+3O2
2CO2+2H2O,C2H2+
O2
2CO2+H2O,恢复到原来的温度和压强,根据反应方程式可知,CH4和C2H4反应前后气体总体积不变,体积减小由乙炔燃烧导致,根据差量法计算乙炔的体积,进而计算炔的体积分数.
| ||
| ||
| 5 |
| 2 |
| ||
解答:
解:恢复到原来的温度和压强,水为气体,则:
CH4+2O2
CO2+2H2O?△V
1 2 1 2 0
C2H4+3O2
2CO2+2H2O?△V
1 3 2 2 0
C2H2+
O2
2CO2+H2O△V
1 2.5 2 1 0.5
CH4和C2H4反应前后气体体积不变,体积减小由乙炔燃烧导致,
设混合气体中C2H2为ymL,则:
C2H2+
O2
2CO2+H2O△V
1 2.5 2 1 0.5
ymL 8mL
所以1:0.5=ymL:8mL,解得y=16
则原混合烃中乙炔的体积分数为
×100%=50%,
故选C.
CH4+2O2
| ||
1 2 1 2 0
C2H4+3O2
| ||
1 3 2 2 0
C2H2+
| 5 |
| 2 |
| ||
1 2.5 2 1 0.5
CH4和C2H4反应前后气体体积不变,体积减小由乙炔燃烧导致,
设混合气体中C2H2为ymL,则:
C2H2+
| 5 |
| 2 |
| ||
1 2.5 2 1 0.5
ymL 8mL
所以1:0.5=ymL:8mL,解得y=16
则原混合烃中乙炔的体积分数为
| 16mL |
| 32mL |
故选C.
点评:本题考查混合物计算、化学方程式有关计算,关键是根据方程式判断体积变化,确定体积减小由乙炔燃烧导致,注意差量法的应用,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
有机物的种类繁多,但其命中是有规则的.下列有机物命名正确的是( )
A、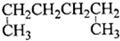 1,4-二甲基丁烷 1,4-二甲基丁烷 |
B、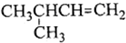 3-甲基丁烯 3-甲基丁烯 |
C、 2-甲基丁烷 2-甲基丁烷 |
| D、CH2Cl-CH2Cl 二氯乙烷 |
下列氧化还原反应中,实际参加反应的氧化剂与还原剂物质的量之比正确的是( )
①2H2S+SO2=3S+2H2O; 2:1
②6HNO3(浓)+S=H2SO4+6NO2+2H2O; 1:6
③Fe+4HNO3=Fe(NO3)3+NO+2H2O; 1:1
④2Al+2NaOH+2H2O=2NaAlO2+3H2↑; 1:1.
①2H2S+SO2=3S+2H2O; 2:1
②6HNO3(浓)+S=H2SO4+6NO2+2H2O; 1:6
③Fe+4HNO3=Fe(NO3)3+NO+2H2O; 1:1
④2Al+2NaOH+2H2O=2NaAlO2+3H2↑; 1:1.
| A、只有①正确 | B、③④ |
| C、只有③ | D、①②③④都正确 |
某学生测定CuSO4?xH2O晶体的x值,数据如下(已知x的理论值为5.0):
产生误差的可能原因是( )
| 坩埚质量 | 坩埚+试样 | 失水后,坩埚+试样 |
| 11.70g | 20.82g | 16.02g |
| A、硫酸铜晶体中含不挥发杂质 |
| B、加热时有晶体溅出 |
| C、实验前,晶体表面有吸附水 |
| D、未做恒重操作 |
下列物质属于电解质的是( )
| A、Cu |
| B、液态NH3 |
| C、CO2 |
| D、Na2O2固体 |
将淀粉与KI的混合液装在半透膜中,浸泡在盛有蒸馏水的烧杯中,过一段时间后,取烧杯中的液体进行实验,能证明半透膜有破损的是( )
| A、加入碘水不变蓝色 |
| B、加入碘水变蓝色 |
| C、加入AgNO3溶液不产生黄色沉淀 |
| D、加入AgNO3溶液产生黄色沉淀 |
下列物质属于糖类且属于高分子化合物的是( )
| A、蔗糖 | B、牛油 |
| C、纤维素 | D、蛋白质 |
下列实验设计、操作或实验现象均正确的是( )
| A、检验甲酸中是否混有甲醛,可向样品中加入足量NaOH溶液以中和HCOOH,再做银镜反应实验 |
| B、实验室制取乙酸乙酯时,将反应产生的蒸气经导管通入到饱和烧碱溶液中 |
| C、液态溴乙烷中加入AgNO3溶液观察有无淡黄色沉淀生成,以检验溴元素的存在 |
| D、实验室制硝基苯要在水浴的热水中插入温度计 |
