题目内容
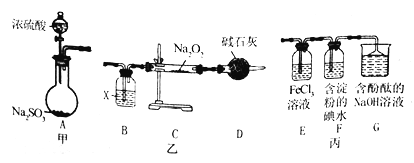
【题目】某兴趣小组运用下图所示组合装置(部分夹持装置未画出)进行探究实验
请回答下列问题:
(1)A同学将甲、乙装置组合进行进行实验,其实验目的是探究______反应的生成物;在连接好装置后,首先要进行的实验操作为____________。
(2)为检验C装置中反应生成物是否有氧气,装置B中盛放的试剂X应为______,装置D中碱石灰的作用是 _______;实验操作及现象是______。
(3)b同学将甲、丙装置组合进行实验,能说明I-的还原性弱于 SO2的现象为_____,发生反应的离子方程式是________。
(4)装置G中的现象是________,说明SO2具有____________性。
(5)为验证装置中SO2与FeCl3发生了氧化还原反应,C同学设计了两套方案,完成下表:
实验操作 | 实验现象 | 实验结论 | |
方案1 | 取少量装置E中的溶液于试管中,向其中滴加____溶液 | 产生白色沉淀 | SO2与FeCl3发生氧化还原反应 |
方案2 | 取少量装置E中的溶液于试管中,向其中滴加 ____溶液 | ____________ |
【答案】 SO2与Na2O2 检查装置的气密性 浓硫酸 吸收未反应的SO2,防止污染空气,同时防止空气中的水蒸气进入装置与Na2O2反应,干扰实验 将带火星的木条放在干燥管D出口处,若木条复燃,则有氧气生成,否则无氧气生成 装置F中溶液蓝色褪去 SO2+I2+2H2O=2I-+SO42-+4H+ 红色褪去 酸性 【答题空10】盐酸酸化的BaCl2 KSCN 溶液不变红
【解析】(1)A同学将甲、乙装置组合进行进行实验,甲装置利用亚硫酸钠与浓硫酸反应制取二氧化硫,气体干燥后进入乙装置与过氧化钠反应,故其实验目的是探究SO2与Na2O2反应的生成物;实验过程有气体的参与,在连接好装置后,首先要进行的实验操作为检查装置的气密性;(2)装置B中盛放浓硫酸,将通入的二氧化硫进行干燥,以免水蒸气进入装置乙中与过氧化钠反应生成氧气而引起干扰;装置D中碱石灰的作用是吸收未反应的SO2,防止污染空气,同时防止空气中的水蒸气进入装置与Na2O2反应,干扰实验;氧气的检验可将带火星的木条放在干燥管D出口处,若木条复燃,则有氧气生成,否则无氧气生成;(3)b同学将甲、丙装置组合进行实验, I-的还原性弱于 SO2,则碘单质被二氧化硫还原,现象为装置F中溶液蓝色褪去;发生反应的离子方程式是SO2+I2+2H2O=2I-+SO42-+4H+;(4)装置G中含有酚酞的氢氧化钠溶液呈红色,当过量的二氧化硫被吸收后溶液碱性减弱,现象是溶液红色褪去;说明SO2具有酸性;(5)方案1取少量装置E中的溶液于试管中,向其中滴加盐酸酸化的BaCl2,产生白色沉淀,证明溶液中含有硫酸根离子;方案2取少量装置E中的溶液于试管中,向其中滴加KSCN,溶液不变红,证明溶液中的铁离子已被还原为亚铁离子,从而证明二氧化硫与氯化铁发生了氧化还原反应生成了氯化亚铁、硫酸和盐酸。