题目内容
【题目】分类是学习和研究化学物质及其变化的一种常用的科学方法。
(1)下列4组物质中均有一种物质的主要化学性质与其他3种不同。
A、CaO、Na2O、CO2、MgO B、CH3COOH、H2SO4、Ba(OH)2、HNO3
C、H2、Cl2、P、Cu D、HCl、CH3CH2OH、H2SO4、HNO3
①写出D组中不同于其他三种的物质的化学式:________。
②A组中的一种物质与B组中的—种物质反应的量不同产物有所不同。写出这两种物质反应有沉淀产生的离子反应方程式:_______。
③C组中Cu在一定条件下可与H2、Cl2、P等化合。写出 CuH在Cl2中燃烧的化学方程式:_________________。
(2)NaOH、Na2CO3、NaA1O2溶液都具有碱性。向500mL由NaOH、Na2CO3、NaA1O2组成的混合溶液中滴加0.2molL-1盐酸,所消耗盐酸体积如图所示,回答下列问题:
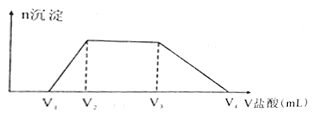
①写出加盐酸V1至 V2段反应的离子方程式:___________。
②用 36.5%(密度为1.19gmL-1) 的浓盐酸配制945mL0.2molL-1盐酸,需要量取的浓盐酸体积为_________________。
③若V1=50 mL,V2=100 mL,V3=200 mL,则V4= ______。原混合溶液中NaOH、Na2CO3、NaA1O2的物质的量之比为_________。
【答案】 CH3CH2OH CO2+Ba2++2OH-=BaCO3↓+H2O 2CuH+3Cl2![]() 2CuCl2+2HCl AlO2-+H++H2O=Al(OH)3↓ 16.81mL 350mL 1:1:1
2CuCl2+2HCl AlO2-+H++H2O=Al(OH)3↓ 16.81mL 350mL 1:1:1
【解析】(1)①D组中HCl、H2SO4、HNO3都为强酸,强电解质,而CH3CH2OH是非电解质,故不同于其他三种的物质的化学式:CH3CH2OH;②结合各物质性质可知,A组中的一种物质CO2与B组中的—种物质Ba(OH)2反应的量不同产物有所不同。这两种物质反应有沉淀产生的离子反应方程式为:CO2+Ba2++2OH-=BaCO3↓+H2O;③CuH在Cl2中燃烧生成氯化铜和氯化氢,反应的化学方程式:2CuH+3Cl2 ![]() 2CuCl2+2HCl;(2)①加盐酸V1至 V2段反应产生沉淀且沉淀量达到最大,故发生反应的离子是偏铝酸根离子,反应的离子方程式为:AlO2-+H++H2O=Al(OH)3↓;②配制945mL0.2molL-1盐酸,需要用1000 mL容量瓶配制,用 36.5%(密度为1.19gmL-1)的浓盐酸配制1000mL0.2molL-1盐酸,设需要量取的浓盐酸体积为VmL,则1L×0.2molL-1=
2CuCl2+2HCl;(2)①加盐酸V1至 V2段反应产生沉淀且沉淀量达到最大,故发生反应的离子是偏铝酸根离子,反应的离子方程式为:AlO2-+H++H2O=Al(OH)3↓;②配制945mL0.2molL-1盐酸,需要用1000 mL容量瓶配制,用 36.5%(密度为1.19gmL-1)的浓盐酸配制1000mL0.2molL-1盐酸,设需要量取的浓盐酸体积为VmL,则1L×0.2molL-1=![]() ,解得:V=16.8mL;③根据反应AlO2-+H++H2O=Al(OH)3↓,Al(OH)3+3H+=Al3++3H2O,产生沉淀和溶解沉淀所需要的盐酸的体积之比为1:3,则V4=200 mL+50 mL×3= 350mL;再根据反应OH-+H+=H2O,CO32-+2H+=H2O+CO2↑,盐酸与NaOH、Na2CO3、NaA1O2溶液反应时分别所用体积之比为1:2:1,则NaOH、Na2CO3、NaA1O2物质的量之比为1:1:1。
,解得:V=16.8mL;③根据反应AlO2-+H++H2O=Al(OH)3↓,Al(OH)3+3H+=Al3++3H2O,产生沉淀和溶解沉淀所需要的盐酸的体积之比为1:3,则V4=200 mL+50 mL×3= 350mL;再根据反应OH-+H+=H2O,CO32-+2H+=H2O+CO2↑,盐酸与NaOH、Na2CO3、NaA1O2溶液反应时分别所用体积之比为1:2:1,则NaOH、Na2CO3、NaA1O2物质的量之比为1:1:1。

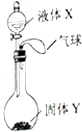
【题目】如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.如表中液体X和固体Y的组合,不符合题意的是( )
① | ② | ③ | ④ | |
X | 水 | 水 | 稀硫酸 | 双氧水 |
Y | 硝酸铵 | 氢氧化钠 | 氯化钠 | 二氧化锰 |
A.①③
B.②④
C.①②
D.③④
【题目】某兴趣小组运用下图所示组合装置(部分夹持装置未画出)进行探究实验
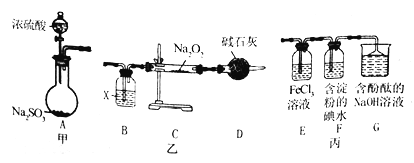
请回答下列问题:
(1)A同学将甲、乙装置组合进行进行实验,其实验目的是探究______反应的生成物;在连接好装置后,首先要进行的实验操作为____________。
(2)为检验C装置中反应生成物是否有氧气,装置B中盛放的试剂X应为______,装置D中碱石灰的作用是 _______;实验操作及现象是______。
(3)b同学将甲、丙装置组合进行实验,能说明I-的还原性弱于 SO2的现象为_____,发生反应的离子方程式是________。
(4)装置G中的现象是________,说明SO2具有____________性。
(5)为验证装置中SO2与FeCl3发生了氧化还原反应,C同学设计了两套方案,完成下表:
实验操作 | 实验现象 | 实验结论 | |
方案1 | 取少量装置E中的溶液于试管中,向其中滴加____溶液 | 产生白色沉淀 | SO2与FeCl3发生氧化还原反应 |
方案2 | 取少量装置E中的溶液于试管中,向其中滴加 ____溶液 | ____________ |