题目内容
15.500ml 0.4mol/L的盐酸溶液中含HCl0.2mol,相当于标准状况下由4.48 LHCl溶于水配制而成,其中含HCl7.3g,与0.2 mol/L的CaCl2溶液中Cl-浓度相等,从该溶液中取出20毫升溶液,加水稀至80毫升,稀释后溶液的物质的量浓度是:0.1mol/L.分析 根据n=cv计算500ml 0.4mol/L的盐酸溶液中含HCl的物质的量,根据v=nVm计算HCl标准状况下的体积,根据m=nM计算HCl的质量,HCl是强电解质,完全电离,氯离子物质的量等于HCl的物质的量;c(Cl-)=c(HCl)、c(Cl-)=2c(CaCl2)计算Cl-浓度相等的CaCl2溶液的浓度,从该溶液中取出20毫升溶液,加水稀至80毫升,根据稀释定律求解稀释后溶液的物质的量浓度.
解答 解:500ml 0.4mol/L的盐酸溶液中含HCl的物质的量n=cv=0.4mol/L×0.5L=0.2mol,HCl标准状况下的体积v=nVm=0.2mol×22.4L/mol=4.48L,含HCl质量为m=nM=0.2mol×36.5g/mol=7.3g,盐酸中c(Cl-)=c(HCl)=0.4mol/L,CaCl2溶液中c(Cl-)=2c(CaCl2),所以Cl-浓度相等的CaCl2溶液的浓度0.2mol/L,从该溶液中取出20毫升溶液,加水稀至80毫升,稀释后溶液的物质的量浓度,根据C浓×V浓=C稀×V稀,0.4mol/L×20ml=C稀×80ml,解得:C稀=0.1mol/L,
故答案为:0.2;4.48;7.3;0.2;0.1mol/L.
点评 本题考查物质的量的有关计算,侧重考查计算能力,明确物质的量公式中各个物理量的关系即可解答,题目难度不大.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | 食盐、稀醋酸和蔗糖都是电解质 | |
| B. | 甲烷和乙烯均可使酸性KMnO4溶液褪色 | |
| C. | 纤维素、淀粉和蛋白质都是高分子化合物 | |
| D. | 乙酸乙酯和植物油均可水解生成乙醇 |
10.强酸与强碱稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.向1L 0.5 mol•L-1的NaOH溶液中加入下列物质:①浓硫酸 ②稀硝酸,恰好完全反应的热效应依次为△H1、△H2,则二者的关系正确的是( )
| A. | △H1=△H2 | B. | △H1>△H2 | C. | △H2>△H1 | D. | 无法比较 |
20.把CoCl2溶解于浓盐酸中,溶液中存在下列平衡:Co2++4Cl-?CoCl4-△H>0有关上述可逆反应的下列说法不正确的是( )
| A. | 对溶液所在体系加热,溶液蓝色加深 | |
| B. | 对溶液所在体系用冰水降温,上述反应的平衡常数减小 | |
| C. | 室温下,加水稀释至一定范围,溶液为蓝色 | |
| D. | 室温下,加水稀释至一定范围,溶液为粉红色 |
7.在下列各指定溶液中,离子可能大量共存的是( )
| A. | 澄清透明的溶液中:Cu2+、Fe3+、NO3-、Cl- | |
| B. | 使红色石蕊试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl- | |
| C. | 含有大量ClO-的溶液中:K+、OH-、I-、SO32- | |
| D. | c(Fe3+)=0.1 mol•L-1的溶液中:K+、ClO-、SO42-、SCN- |
5.下列有关物质的性质和应用正确的是( )
| A. | 福尔马林可用于保存海鲜产品 | |
| B. | 油脂在酸性条件下可水解生成高级脂肪酸和甘油 | |
| C. | 淀粉、油脂、氨基酸都能水解,但水解产物不同 | |
| D. | 合成橡胶与光导纤维都属于有机高分子材料 |


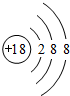 ,非金属性最强的元素是F,最高价氧化物的水化物碱性最强的碱的电子式是
,非金属性最强的元素是F,最高价氧化物的水化物碱性最强的碱的电子式是 ,最高价氧化物的水化物酸性最强的酸的化学式是HClO4;
,最高价氧化物的水化物酸性最强的酸的化学式是HClO4; .
.