题目内容
在一密闭容器中,反应aA(g)?bB(g)达平衡(Ⅰ).保持稳定不变,将容器体积增加一倍,当达到新的平衡(Ⅱ)时,实验测得cB(Ⅱ):cB(Ⅰ)=2:5,则下列说法正确的是( )
| A、平衡向正反应方向移动 |
| B、a<b |
| C、物质B的质量分数增加 |
| D、物质A的转化率降低 |
考点:化学平衡的计算
专题:
分析:将容器体积增加一倍,若平衡不移动,cB(Ⅱ):cB(Ⅰ)=2.5:5,而当达到新平衡时,实验测得cB(Ⅱ):cB(Ⅰ)=2:5,则体积增大,相当于压强减小,平衡逆向移动,以此来解答.
解答:
解:保持温度不变,将容器体积增加一倍,当达到新平衡时,实验测得cB(Ⅱ):cB(Ⅰ)=2:5,相当于压强减小,平衡逆向移动,
A.平衡逆向移动,故A错误;
B.减小压强,平衡逆向移动即平衡向体积增大的方向移动,所以a>b,故B错误;
C.减小压强,平衡逆向移动,B的质量减小,反应中气体的质量不变,则B的质量分数变小,故C错误;
D.平衡逆向移动,物质A的转化率减小,故D正确;
故选:D.
A.平衡逆向移动,故A错误;
B.减小压强,平衡逆向移动即平衡向体积增大的方向移动,所以a>b,故B错误;
C.减小压强,平衡逆向移动,B的质量减小,反应中气体的质量不变,则B的质量分数变小,故C错误;
D.平衡逆向移动,物质A的转化率减小,故D正确;
故选:D.
点评:本题考查压强对反应速率及平衡的影响,注意利用体积变化分析出压强对化学平衡的影响即可解答,把握静态变化与动态变化的结合,题目难度不大.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
下列说法或表达正确的是( )
①次氯酸的结构式为 H-Cl-O
②含有离子键的化合物都是离子化合物
③蛋白质、漂白粉、苛性钾、液氨分别为纯净物、混合物、强电解质和非电解质
④丁达尔效应可用于区别溶液和胶体,云、雾均能产生丁达尔效应
⑤酸性氧化物不一定是非金属氧化物,但是碱性氧化物一定是金属氧化物.
①次氯酸的结构式为 H-Cl-O
②含有离子键的化合物都是离子化合物
③蛋白质、漂白粉、苛性钾、液氨分别为纯净物、混合物、强电解质和非电解质
④丁达尔效应可用于区别溶液和胶体,云、雾均能产生丁达尔效应
⑤酸性氧化物不一定是非金属氧化物,但是碱性氧化物一定是金属氧化物.
| A、①②④ | B、①③⑤ |
| C、②④⑤ | D、③④⑤ |
在18世纪70年代,首先发现并制得氯气的化学家是( )
| A、舍勒 | B、戴维 | C、玻尔 | D、侯德榜 |
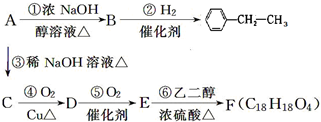
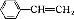 大36.5,请回答:
大36.5,请回答: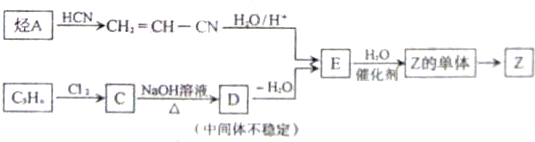

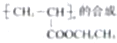 实验,此实验过程涉及的反应类型有
实验,此实验过程涉及的反应类型有 某同学利用如图装置实现铜与浓、稀硝酸反应,过程如下:
某同学利用如图装置实现铜与浓、稀硝酸反应,过程如下: